Масса химических элементов во вселенной
Достаточно надёжно описываемые формы материи, которые хорошо известны, составляют всего несколько процентов от общей плотности космологической материи. Изучение новых форм материи − темной материи и темной энергии − важнейшая проблема современной физики.
Академик А. М. Черепащук: «Начиная от первых наивных представлений об устройстве Вселенной (X в. до н.э.) человечество в стремлении понять природу окружающего нас мира прошло через две научные революции: коперниковскую (переход от геоцентризма к гелиоцентризму) и Эйнштейна — Фридмана — Хаббла (переход от модели статической Вселенной к модели расширяющейся, эволюционирующей, Вселенной). Сейчас мы стоим на пороге третьей революции в астрономии (открытие ускоренного расширения Вселенной и осознание того факта, что барионная материя − это лишь малая добавка к общей плотности всех видов материи во Вселенной).
Современная космология берёт своё начало с первых десятилетий XX в. За почти 100 лет своего существования, считая от первых наблюдений Слайфера и космологической работы Эйнштейна, космология превратилась из области абстрактных и иногда близких к фантастическим рассуждений в одно из центральных направлений естествознания XXI в. Сегодня космология обладает прочным наблюдательным фундаментом, на основе которого развивается теория, основанная на достижениях современной физики, включая общую теорию относительности, ядерную физику и физику элементарных частиц. Особо следует отметить недавнее открытие бозона Хиггса на Большом адронном коллайдере, что может дать новый импульс развитию теоретических исследований в области космологии.
Космология ставит новые проблемы, выдвигает новые идеи и гипотезы, делает смелые предсказания, которые находятся на переднем крае науки, и даёт широкую и богатую картину окружающего нас мира, ставшую уже неотъемлемой частью общей культуры человечества».
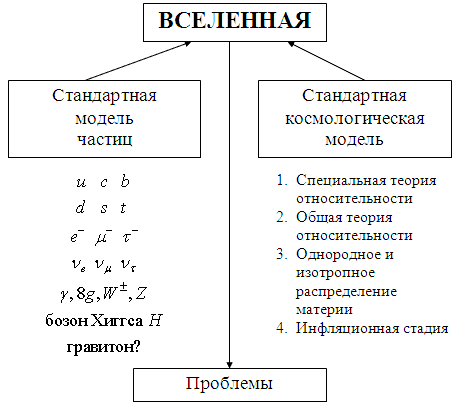
Сегодняшнее описание окружающего нас мира схематически показано на диаграмме (рис. 60).
- Природа темной материи
- Природа темной энергии
- Стабильность протона
- Асимметрия вещество-антивещество
- Почему существуют три поколения фундаментальных частиц
- состоящих из пары кварков и лептонов?
- Существуют ли четвертое, пятое. поколения фундаментальных частиц?
- Почему существуют кварки и лептоны. и чем вызвано различие между ними?
- Почему фундаментальными частицами вещества являются фермионы. в то время как фундаментальными переносчиками взаимодействия − бозоны?
- Почему разные фундаментальные частицы имеют разные массы?
- Почему различаются пространственная и временная степени свободы?
- Живем ли мы в четырехмерном пространстве-времени, или оно имеет большее число измерений?
- Существуют ли кванты пространства и времени?
Рис. 60. Проблемы современной модели Вселенной
Современное представление об эволюции Вселенной приведено в таблице 21. Стандартная модель хорошо описывает все известные частицы и взаимодействия между ними. Стандартная космологическая модель, базирующаяся на специальной и общей теории относительности, в целом правильно описывает динамику материи во Вселенной. Расширение Вселенной началось с инфляционной стадии Большого взрыва. Инфляционная стадия привела к образованию однородной и изотропной Вселенной. Вслед за стадией инфляции произошли рождение и аннигиляция частиц, образование протонов, нейтронов, гелия во время дозвездного нуклеосинтеза, образование реликтового излучения. Реликтовое излучение дает информацию о состоянии Вселенной в возрасте 300 тыс. лет.
Источник
7 самых тяжелых элементов на Земле | По атомной массе
Мы должны быть более конкретными, когда говорим о том, насколько тяжелый элемент. Есть два возможных способа определения «самых тяжелых» элементов — на основе их плотности или атомной массы.
Самый тяжелый элемент с точки зрения плотности можно определить как массу на единицу объема, которая обычно измеряется в граммах на кубический сантиметр или килограммах на кубический метр.
Самым плотным природным элементом на Земле является осмий. Это блестящее вещество имеет плотность 22,59 г / см3, чуть больше, чем у иридия.
Другой способ взглянуть на тяжесть — это атомный вес, средняя масса атомов элемента. Стандартная единица атомной массы составляет одну двенадцатую от массы одного атома углерода-12.
Это фундаментальное понятие в химии, потому что большинство химических реакций происходит в соответствии с простыми числовыми соотношениями между атомами. Ниже мы перечислили 7 самых тяжелых элементов, найденных на Земле в соответствии с их атомными массами.
Примечание: мы не упомянули элементы, свойства которых неизвестны или еще не подтверждены, такие как московия, флеровия, нихония и мейтнерия.
7. Резерфордий
Атомная масса: 267
Резерфордий (Rf) был первым сверхтяжелым элементом, который был обнаружен [в 1964 году]. Он очень радиоактивен, и его самый стабильный изотоп 267Rf имеет период полураспада около 78 минут.
Резерфордий — это искусственный элемент, созданный в лаборатории путем бомбардировки калифорния-249 ядрами углерода-12. Всего было зарегистрировано 16 изотопов с атомными массами между 253 и 270. Большинство из них быстро распадаются через пути самопроизвольного деления.
Ожидается, что этот элемент будет твердым при нормальных условиях и предположительно будет иметь химические свойства, подобные гафнию. Он был создан только в незначительных количествах и используется только для научных исследований.
6. Дубний
Атомная масса: 268
Дубний (Db) — радиоактивный элемент, впервые синтезированный в 1968 году в Объединенном институте ядерных исследований, Россия. Он имеет семь признанных изотопов, из которых наиболее стабильным является 268Db с периодом полураспада 32 часа.
Дубний можно получить бомбардировкой калифорния-249 азотом или америция-243 неоном. Ограниченный анализ химии Дубния подтвердил, что этот элемент ведет себя больше как ниобий, а не тантал, нарушая периодические тенденции.
Поскольку элемент не найден в природе свободным и не создан в больших количествах в лаборатории, у него нет других применений, кроме научных исследований.
5. Сиборгиум
Атомная масса: 269
Seaborgium (Sg) был впервые синтезирован в 1974 году в лаборатории Лоуренса в Беркли, штат Калифорния. Исследовательская группа подвергла бомбардировке калифорний-249 ядрами кислорода-18 для получения сиборгия-263.
Это радиоактивный элемент, чей самый стабильный изотоп (269Sg) имеет период полураспада около 14 минут. Только несколько атомов сиборгия когда-либо были произведены, и его использование исключительно для научных исследований.
Небольшое исследование, проведенное на этом синтетическом химическом элементе, указывает на то, что сиборгий является плотным тяжелым металлом в нормальных условиях.
В 2014 году японские исследователи впервые установили химическую связь между атомом углерода и сиборгием, открывая новые двери для анализа влияния относительности Эйнштейна на структуру периодической таблицы.
4. Борий
Атомная масса: 270
Bohrium (Bh) — это искусственно созданный радиоактивный элемент, названный в честь известного физика Нильса Бора. Он синтезируется путем бомбардировки висмута ионами хрома.
Поскольку он очень быстро разлагается за счет испускания альфа-частиц (период полураспада 270Bh составляет 61 секунду), изучать этот элемент очень сложно.
Борий не встречается в природе, и только несколько атомов были получены до настоящего времени. Возможно, он никогда не будет изолирован в наблюдаемых количествах.
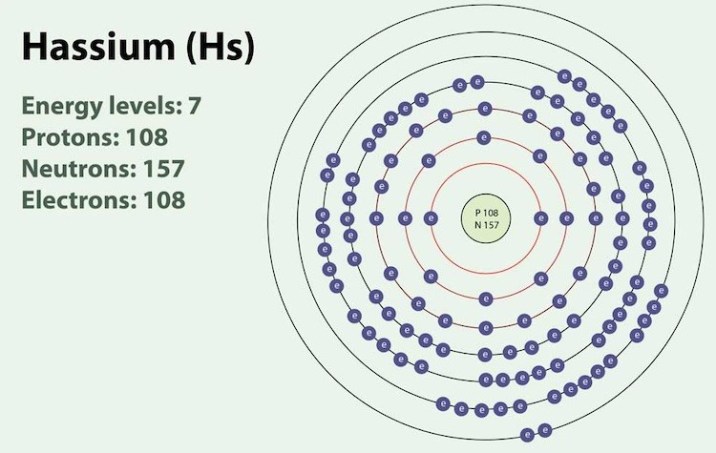
3. Хассий
Атомная масса: 270
Обнаруженный немецкими физиками в 1984 году, калий (Hs) является одним из самых тяжелых и плотных элементов периодической таблицы. Все 9 изотопов элемента имеют очень короткие периоды полураспада: самый стабильный (270Hs) имеет период полураспада 10 секунд.
Пока что получено всего несколько атомов хасция. Таким образом, его свойства еще не известны. Хотя точная температура плавления, температура кипения и плотность не подтверждены, элемент считается твердым при комнатной температуре.
Этот радиоактивный переходный металл может реагировать с другими элементами [своей группы], если он производится в больших количествах. На данный момент он не имеет коммерческого использования, кроме научных исследований.
2. Tennessine
Атомная масса: 294
Tennessine (Ts) является вторым наиболее тяжелым известным элементом, обнаруженным российско-американским коллаборацией в 2010 году. Это радиоактивный, искусственно произведенный элемент. Хотя его классификация неизвестна, ожидается, что он будет надежным.
Теннессин был получен реакцией синтеза кальция-48 с берклием-249. Во всех проведенных экспериментах его атомы длились десятки и сотни миллисекунд.
Использование tennessine ограничено исследовательскими целями из-за его незначительного производства. Его самый стабильный изотоп (294Ts) имеет период полураспада около 80 миллисекунд, который распадается из-за альфа-распада.
1. Оганесон
Атомная масса: 294
Впервые синтезированный в 2002 году, Oganesson (Og) — самый тяжелый элемент периодической таблицы. Этот высокорадиоактивный элемент является членом группы благородных газов. Удивительно, но это первый благородный газ, который химически реактивен.
С 2005 года было идентифицировано только 6 атомов Oganesson. Он проявляет очень необычные физические и химические свойства, большинство из которых еще недостаточно изучены.
Поскольку Oganesson очень нестабилен (с периодом полураспада около 0,89 миллисекунд) и не происходит естественным путем, почти нет причин для рассмотрения его опасности для здоровья.
Тяжелый элемент природного происхождения: Уран
Урановое стекло светится под ультрафиолетовым светом | Предоставлено: Wikimedia Commons.
Атомная масса: 238,0289
На протяжении более 6 десятилетий уран (U) использовался в качестве богатого источника концентрированной энергии. Это самый тяжелый элемент в земной коре, он встречается в 500 раз чаще, чем золото, и в 40 раз чаще, чем серебро.
Хотя уран является радиоактивным элементом, скорость его распада значительно ниже, чем у других элементов, связанных с радиоактивностью. Его наиболее естественная форма (уран-238) имеет период полураспада около 4,5 миллиардов лет.
Уран в основном используется в качестве ядерного топлива для производства электроэнергии на атомных электростанциях. Один килограмм урана-235 может генерировать около 80 тераджоулей энергии, что эквивалентно энергии, генерируемой 3000 тонн угля.
Это чрезвычайно токсичный элемент: прием соединений шестивалентного урана может привести к повреждению иммунной системы и врожденным дефектам.
Источник
Обилие химических элементов — Abundance of the chemical elements
Обилие химических элементов является мерой возникновения из химических элементов относительно всех других элементов в данной среде. Численность измеряется одним из трех способов: массовая доля (то же, что и массовая доля); по мольной доле (доля атомов в числовом исчислении, а иногда и доля молекул в газах); или по объемной доле . Объемная доля — это обычная мера содержания в смешанных газах, таких как атмосферы планет, и аналогична по величине молекулярной мольной доле для газовых смесей при относительно низких плотностях и давлениях, а также в идеальных газовых смесях. Большинство значений численности в этой статье даны в массовых долях.
Например, содержание кислорода в чистой воде можно измерить двумя способами: массовая доля составляет около 89%, потому что это доля массы воды, которая является кислородом. Однако мольная доля составляет около 33%, потому что только 1 атом из 3 в воде, H 2 O, является кислородом. В качестве другого примера, глядя на масс-фракции обилие водорода и гелия в обоих Вселенной в целом и в атмосфере из газовых гигантских планет , таких как Юпитер , это 74% для водорода и 23-25% для гелия ; в то время как (атомная) мольная доля водорода в этих средах составляет 92%, а гелия — 8%. Изменение данной среды на внешнюю атмосферу Юпитера , где водород двухатомный, а гелий нет, изменяет молекулярную мольную долю (долю от общего количества молекул газа), а также долю атмосферы по объему водорода примерно до 86%, и гелия до 13%.
Изобилие химических элементов во Вселенной определяется большим количеством водорода и гелия, которые были произведены в результате Большого взрыва . Остальные элементы, составляющие лишь около 2% Вселенной, в основном были произведены сверхновыми и некоторыми красными звездами-гигантами . Литий , бериллий и бор встречаются редко, потому что, хотя они производятся в результате ядерного синтеза, они затем разрушаются другими реакциями в звездах. Элементов от углерода до железа относительно больше во Вселенной из-за простоты их получения в процессе нуклеосинтеза сверхновых . Элементы с более высоким атомным номером, чем железо (элемент 26), становятся все более редкими во Вселенной, потому что при их производстве они все больше поглощают звездную энергию. Кроме того, элементы с четными атомными номерами обычно более распространены, чем их соседи в периодической таблице , из-за благоприятной энергетики образования.
Обилие элементов на Солнце и на внешних планетах такое же, как и во Вселенной. Из-за солнечного нагрева элементы Земли и внутренних каменистых планет Солнечной системы претерпели дополнительное истощение летучих водорода, гелия, неона, азота и углерода (который улетучивается в виде метана). Кора, мантия и ядро Земли демонстрируют признаки химической сегрегации плюс некоторая секвестрация по плотности. Более легкие силикаты алюминия находятся в коре, больше силиката магния в мантии, в то время как металлическое железо и никель составляют ядро. Обилие элементов в специализированных средах, таких как атмосфера, океаны или человеческое тело, в первую очередь является продуктом химического взаимодействия со средой, в которой они находятся.
СОДЕРЖАНИЕ
Вселенная
| Z | Элемент | Массовая доля (ppm) |
|---|---|---|
| 1 | Водород | 739 000 |
| 2 | Гелий | 240 000 |
| 8 | Кислород | 10 400 |
| 6 | Углерод | 4600 |
| 10 | Неон | 1,340 |
| 26 год | Утюг | 1,090 |
| 7 | Азот | 960 |
| 14 | Кремний | 650 |
| 12 | Магний | 580 |
| 16 | Сера | 440 |
| Общее | 999 500 |
Элементы, то есть обычная ( барионная ) материя, состоящая из протонов , нейтронов и электронов , составляют лишь небольшую часть содержимого Вселенной . Космологические наблюдения показывают, что только 4,6% энергии Вселенной (включая массу, вносимую энергией, E = mc² ↔ m = E / c²) составляет видимую барионную материю, из которой состоят звезды , планеты и живые существа. Остальное, как полагают, состоит из темной энергии (68%) и темной материи (27%). Это формы материи и энергии, которые, как считается, существуют на основе научной теории и индуктивных рассуждений, основанных на наблюдениях, но они не наблюдались напрямую, и их природа не совсем понятна.
Наиболее стандартная (барионная) материя находится в межгалактическом газе, звездах и межзвездных облаках в форме атомов или ионов ( плазма ), хотя ее можно найти в вырожденных формах в экстремальных астрофизических условиях, таких как высокие плотности внутри белых карликов. и нейтронные звезды .
Водород — самый распространенный элемент во Вселенной; гелий на втором месте. Однако после этого ранг изобилия больше не соответствует порядковому номеру ; кислород имеет степень распространенности 3, но атомный номер 8. Все остальные встречаются значительно реже.
Обилие самых легких элементов хорошо предсказывается стандартной космологической моделью , поскольку они в основном образовались вскоре (то есть в течение нескольких сотен секунд) после Большого взрыва в процессе, известном как нуклеосинтез Большого взрыва . Более тяжелые элементы в основном были произведены гораздо позже, внутри звезд .
По оценкам, водород и гелий составляют примерно 74% и 24% всей барионной материи во Вселенной соответственно. Несмотря на то, что они составляют лишь очень небольшую часть Вселенной, оставшиеся «тяжелые элементы» могут сильно влиять на астрономические явления. Только около 2% (по массе) диска галактики Млечный Путь состоит из тяжелых элементов.
Эти другие элементы создаются звездными процессами. В астрономии «металл» — это любой элемент, кроме водорода или гелия. Это различие важно, потому что водород и гелий — единственные элементы, которые были произведены в значительных количествах во время Большого взрыва. Таким образом, Металличность из галактики или другого объекта является показателем звездной активности после Большого взрыва.
В общем, элементы вплоть до железа образуются в больших звездах в процессе превращения в сверхновые . Железо-56 особенно распространено, так как это наиболее стабильный нуклид (в том смысле, что он имеет самую высокую ядерную энергию связи на нуклон) и может быть легко получен из альфа-частиц (являясь продуктом распада радиоактивного никеля-56 , в конечном итоге полученного из 14 ядер гелия). Элементы тяжелее железа образуются в процессах поглощения энергии в крупных звездах, и их содержание во Вселенной (и на Земле) обычно уменьшается с увеличением атомного номера.
Солнечная система
| Нуклид | А | Массовая доля в миллионных долях | Фракция атома в миллионных долях |
|---|---|---|---|
| Водород-1 | 1 | 705 700 | 909 964 |
| Гелий-4 | 4 | 275 200 | 88 714 |
| Кислород-16 | 16 | 9 592 | 477 |
| Углерод-12 | 12 | 3032 | 326 |
| Азот-14 | 14 | 1,105 | 102 |
| Неон-20 | 20 | 1,548 | 100 |
 | |||
| Другие нуклиды: | 3 879 | 149 | |
| Кремний-28 | 28 год | 653 | 30 |
| Магний-24 | 24 | 513 | 28 год |
| Утюг-56 | 56 | 1,169 | 27 |
| Сера-32 | 32 | 396 | 16 |
| Гелий-3 | 3 | 35 год | 15 |
| Водород-2 | 2 | 23 | 15 |
| Неон-22 | 22 | 208 | 12 |
| Магний-26 | 26 год | 79 | 4 |
| Углерод-13 | 13 | 37 | 4 |
| Магний-25 | 25 | 69 | 4 |
| Алюминий-27 | 27 | 58 | 3 |
| Аргон-36 | 36 | 77 | 3 |
| Кальций-40 | 40 | 60 | 2 |
| Натрий-23 | 23 | 33 | 2 |
| Утюг-54 | 54 | 72 | 2 |
| Кремний-29 | 29 | 34 | 2 |
| Никель-58 | 58 | 49 | 1 |
| Кремний-30 | 30 | 23 | 1 |
| Утюг-57 | 57 год | 28 год | 1 |
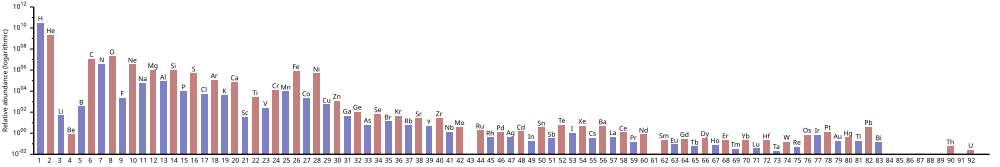
Следующий график (шкала журнала заметок) показывает изобилие элементов в Солнечной системе . В таблице показаны двенадцать наиболее распространенных элементов в нашей галактике (оцененные спектроскопически), измеренные в частях на миллион по массе. Близлежащие галактики, которые развивались по аналогичным направлениям, имеют соответствующее обогащение элементами более тяжелыми, чем водород и гелий. Более далекие галактики рассматриваются такими, какими они были в прошлом, поэтому их содержание элементов кажется более близким к изначальной смеси. Однако, поскольку физические законы и процессы единообразны во всей Вселенной, ожидается, что и в этих галактиках будет одинаковое количество элементов.
Обилие элементов соответствует их происхождению от Большого взрыва и нуклеосинтеза в ряде звезд- прародителей сверхновых . Очень распространенные водород и гелий являются продуктами Большого взрыва, в то время как следующие три элемента встречаются редко, поскольку у них было мало времени, чтобы сформироваться во время Большого взрыва, и они не образуются в звездах (однако они производятся в небольших количествах в результате распада более тяжелых элементов). элементы в межзвездной пыли в результате воздействия космических лучей ).
Начиная с углерода, элементы были произведены в звездах путем накопления из альфа-частиц (ядер гелия), что привело к попеременно большему количеству элементов с четными атомными номерами (они также более стабильны). Эффект того, что химические элементы с нечетными номерами, обычно более редкие во Вселенной, были эмпирически замечены в 1914 году и известны как правило Оддо-Харкинса .
Связь с ядерной энергией связи
Наблюдалась слабая корреляция между оценкой содержания элементов во Вселенной и кривой энергии связи ядер . Грубо говоря, относительная стабильность различных атомных нуклидов оказала сильное влияние на относительное содержание элементов, образовавшихся в результате Большого взрыва , а затем во время развития Вселенной. См. Статью о нуклеосинтезе для объяснения того, как определенные процессы ядерного синтеза в звездах (например, сжигание углерода и т. Д.) Создают элементы тяжелее водорода и гелия.
Еще одна наблюдаемая особенность — неровное чередование относительного содержания и дефицита соседних атомных номеров на кривой содержания элементов и аналогичная картина уровней энергии на кривой энергии связи ядер. Это чередование вызвано более высокой относительной энергией связи (соответствующей относительной стабильности) четных атомных номеров по сравнению с нечетными атомными номерами и объясняется принципом исключения Паули . Массовая формула полуэмпирическое (SEMF), также называемая формула Вейцзеккера или массовая формула Бете-Вайцзекер , дает теоретическое объяснение общей формы кривой ядерной энергии связи.
земля
Земли образуются из того же облака материи, образованное Солнце, но планеты приобрели различные композиции в процессе формирования и эволюции Солнечной системы . В свою очередь, естественная история Земли привела к тому, что части этой планеты имели разную концентрацию элементов.
Масса Земли составляет примерно 5,98 × 10 24 кг. В массе он состоит в основном из железа (32,1%), кислорода (30,1%), кремния (15,1%), магния (13,9%), серы (2,9%), никеля (1,8%), кальция (1,5 %). %) и алюминия (1,4%); оставшиеся 1,2% составляют следовые количества других элементов.
Основной состав Земли по элементарной массе примерно аналогичен валовому составу Солнечной системы, с основными отличиями в том, что на Земле отсутствует большое количество летучих элементов — водорода, гелия, неона и азота, а также углерод, который был утерян в виде летучих углеводородов. Остающийся элементный состав примерно типичен для «каменистых» внутренних планет, которые образовались в тепловой зоне, где солнечное тепло вытеснило летучие соединения в космос. Земля сохраняет кислород как второй по величине компонент своей массы (и наибольшую атомную долю), в основном из-за того, что этот элемент удерживается в силикатных минералах, которые имеют очень высокую температуру плавления и низкое давление пара.
| Атомный номер | Имя | Символ | Массовая доля (ppm) | Атомная доля (ppb) |
|---|---|---|---|---|
| 8 | кислород | О | 297000 | 482 000 000 |
| 12 | магний | Mg | 154000 | 164 000 000 |
| 14 | кремний | Si | 161000 | 150 000 000 |
| 26 год | утюг | Fe | 319000 | 148 000 000 |
| 13 | алюминий | Al | 15900 | 15 300 000 |
| 20 | кальций | Ca | 17100 | 11 100 000 |
| 28 год | никель | Ni | 18220 | 8 010 000 |
| 1 | водород | ЧАС | 260 | 6 700 000 |
| 16 | сера | S | 6350 | 5 150 000 |
| 24 | хром | Cr | 4700 | 2 300 000 |
| 11 | натрий | Na | 1800 | 2 000 000 |
| 6 | углерод | C | 730 | 1,600,000 |
| 15 | фосфор | п | 1210 | 1 020 000 |
| 25 | марганец | Mn | 1700 | 800 000 |
| 22 | титан | Ti | 810 | 440 000 |
| 27 | кобальт | Co | 880 | 390 000 |
| 19 | калий | K | 160 | 110 000 |
| 17 | хлор | Cl | 76 | 56 000 |
| 23 | ванадий | V | 105 | 53 600 |
| 7 | азот | N | 25 | 46 000 |
| 29 | медь | Cu | 60 | 25 000 |
| 30 | цинк | Zn | 40 | 16 000 |
| 9 | фтор | F | 10 | 14 000 |
| 21 год | скандий | Sc | 11 | 6 300 |
| 3 | литий | Ли | 1,10 | 4 100 |
| 38 | стронций | Sr | 13 | 3 900 |
| 32 | германий | Ge | 7.00 | 2,500 |
| 40 | цирконий | Zr | 7.10 | 2 000 |
| 31 год | галлий | Ga | 3,00 | 1,000 |
| 34 | селен | Se | 2,70 | 890 |
| 56 | барий | Ба | 4,50 | 850 |
| 39 | иттрий | Y | 2,90 | 850 |
| 33 | мышьяк | В виде | 1,70 | 590 |
| 5 | бор | B | 0,20 | 480 |
| 42 | молибден | Пн | 1,70 | 460 |
| 44 год | рутений | RU | 1,30 | 330 |
| 78 | платина | Pt | 1,90 | 250 |
| 46 | палладий | Pd | 1,00 | 240 |
| 58 | церий | Ce | 1.13 | 210 |
| 60 | неодим | Nd | 0,84 | 150 |
| 4 | бериллий | Быть | 0,05 | 140 |
| 41 год | ниобий | Nb | 0,44 | 120 |
| 76 | осмий | Операционные системы | 0,90 | 120 |
| 77 | иридий | Ir | 0,90 | 120 |
| 37 | рубидий | Руб. | 0,40 | 120 |
| 35 год | бром | Br | 0,30 | 97 |
| 57 год | лантан | Ла | 0,44 | 82 |
| 66 | диспрозий | Dy | 0,46 | 74 |
| 64 | гадолиний | Б-г | 0,37 | 61 |
| 52 | теллур | Te | 0,30 | 61 |
| 45 | родий | Rh | 0,24 | 61 |
| 50 | банка | Sn | 0,25 | 55 |
| 62 | самарий | См | 0,27 | 47 |
| 68 | эрбий | Э | 0,30 | 47 |
| 70 | иттербий | Yb | 0,30 | 45 |
| 59 | празеодим | Pr | 0,17 | 31 год |
| 82 | Свинец | Pb | 0,23 | 29 |
| 72 | гафний | Hf | 0,19 | 28 год |
| 74 | вольфрам | W | 0,17 | 24 |
| 79 | золото | Au | 0,16 | 21 год |
| 48 | кадмий | CD | 0,08 | 18 |
| 63 | европий | Евросоюз | 0,10 | 17 |
| 67 | гольмий | Хо | 0,10 | 16 |
| 47 | серебро | Ag | 0,05 | 12 |
| 65 | тербий | Tb | 0,07 | 11 |
| 51 | сурьма | Sb | 0,05 | 11 |
| 75 | рений | Re | 0,08 | 10 |
| 53 | йод | я | 0,05 | 10 |
| 69 | тулий | Тм | 0,05 | 7 |
| 55 | цезий | CS | 0,04 | 7 |
| 71 | лютеций | Лу | 0,05 | 7 |
| 90 | торий | Чт | 0,06 | 6 |
| 73 | тантал | Та | 0,03 | 4 |
| 80 | Меркурий | Hg | 0,02 | 3 |
| 92 | уран | U | 0,02 | 2 |
| 49 | индий | В | 0,01 | 2 |
| 81 год | таллий | Tl | 0,01 | 2 |
| 83 | висмут | Би | 0,01 | 1 |
Корка
Массовая доля девяти наиболее распространенных элементов в земной коре составляет приблизительно: кислород 46%, кремний 28%, алюминий 8,3%, железо 5,6%, кальций 4,2%, натрий 2,5%, магний 2,4%, калий 2,0% и титан 0,61%. Остальные элементы составляют менее 0,15%. Для получения полного списка см. Обилие элементов в земной коре .
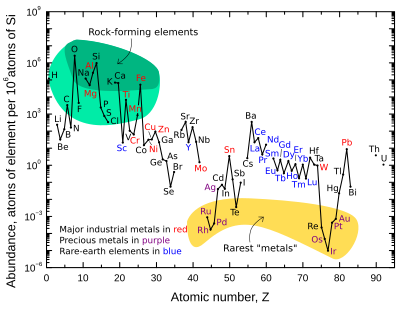
График справа показывает относительное содержание атомов химических элементов в верхней части континентальной коры Земли — части, которая относительно доступна для измерений и оценок.
Многие из элементов, показанных на графике, подразделяются на (частично перекрывающиеся) категории:
- породообразующие элементы (основные элементы в зеленом поле и второстепенные элементы в светло-зеленом поле);
- редкоземельные элементы (лантаноиды, La-Lu, Sc и Y; отмечены синим);
- основные промышленные металлы (мировое производство>
3 × 10 7 кг / год; отмечены красным);
Обратите внимание, что есть два разрыва, где будут находиться нестабильные (радиоактивные) элементы технеций (атомный номер 43) и прометий (атомный номер 61). Эти элементы окружены стабильными элементами, но оба имеют относительно короткий период полураспада (
4 миллиона лет и
18 лет соответственно). Таким образом, они крайне редки, поскольку любые их изначальные первоначальные фракции в материалах до Солнечной системы давно распались. Эти два элемента теперь производятся естественным путем только в результате спонтанного деления очень тяжелых радиоактивных элементов (например, урана , тория или следовых количеств плутония, которые присутствуют в урановых рудах) или в результате взаимодействия некоторых других элементов с космическими лучами . И технеций, и прометий были идентифицированы спектроскопически в атмосферах звезд, где они производятся в ходе продолжающихся процессов нуклеосинтеза.
На графике содержания также есть изломы там, где должны были бы находиться шесть благородных газов , поскольку они не связаны химически в земной коре и генерируются в коре только цепочками распада радиоактивных элементов и поэтому встречаются там крайне редко.
Восемь встречающихся в природе очень редких высокорадиоактивных элементов ( полоний , астат , франций , радий , актиний , протактиний , нептуний и плутоний ) не включены, так как любой из этих элементов, которые присутствовали при формировании Земли, распались эоны назад, а сегодня их количество незначительно и производится только в результате радиоактивного распада урана и тория.
Кислород и кремний — самые распространенные элементы земной коры. На Земле и вообще на каменистых планетах кремний и кислород встречаются гораздо чаще, чем их космическое количество. Причина в том, что они соединяются друг с другом, образуя силикатные минералы . Другие распространенные в космосе элементы, такие как водород , углерод и азот, образуют летучие соединения, такие как аммиак и метан, которые легко улетучиваются в космос из-за высокой температуры образования планет и / или солнечного света.
Редкоземельные элементы
«Редкие» элементы земли — историческое неправильное название. Постоянство этого термина отражает скорее незнакомость, чем истинную редкость. Более распространенные редкоземельные элементы аналогичным образом сконцентрированы в коре по сравнению с обычными промышленными металлами, такими как хром, никель, медь, цинк, молибден, олово, вольфрам или свинец. Два наименее распространенных редкоземельных элемента ( тулий и лютеций ) встречаются почти в 200 раз чаще, чем золото . Однако, в отличие от обычных цветных и драгоценных металлов, редкоземельные элементы имеют очень небольшую тенденцию к концентрации в пригодных для использования рудных месторождениях. Следовательно, большая часть мировых запасов редкоземельных элементов поступает только из нескольких источников. Кроме того, все редкоземельные металлы очень похожи друг на друга по химическому составу, и поэтому их довольно трудно разделить на количества чистых элементов.
Различия в содержании отдельных редкоземельных элементов в верхней континентальной коре Земли представляют собой суперпозицию двух эффектов: ядерного и геохимического. Во-первых, редкоземельные элементы с четными атомными номерами ( 58 Ce, 60 Nd, . ) имеют большее космическое и земное содержание, чем соседние редкоземельные элементы с нечетными атомными номерами ( 57 La, 59 Pr, . ). Во-вторых, более легкие редкоземельные элементы более несовместимы (потому что они имеют больший ионный радиус) и поэтому более сильно сконцентрированы в континентальной коре, чем более тяжелые редкоземельные элементы. В большинстве месторождений редкоземельных руд первые четыре редкоземельных элемента — лантан , церий , празеодим и неодим — составляют от 80% до 99% от общего количества редкоземельного металла, который может быть найден в руде.
Мантия
Массовая доля восьми самых распространенных элементов в мантии Земли (см. Основную статью выше) составляет приблизительно: кислород 45%, магний 23%, кремний 22%, железо 5,8%, кальций 2,3%, алюминий 2,2%, натрий 0,3%. , калий 0,3%.
Основной
В связи с массовой сегрегации , ядро Земли , как полагают, в основном состоит из железа (88,8%), с меньшим количеством никеля (5,8%), серы (4,5%), и менее чем 1% микроэлементов.
Океан
Самыми распространенными элементами в океане по массе в процентах являются кислород (85,84%), водород (10,82%), хлор (1,94%), натрий (1,08%), магний (0,13%), сера (0,09%), кальций (0,04%), калий (0,04%), бром (0,007%), углерод (0,003%) и бор (0,0004%).
Атмосфера
Порядок элементов в атмосфере по объемной доле (что примерно соответствует молекулярной доле) : азот (78,1%), кислород (20,9%), аргон (0,96%), за которым следуют (в неопределенном порядке) углерод и водород, потому что водяной пар и углекислый газ, которые представляют собой большинство из этих двух элементов в воздухе, являются переменными компонентами. Сера, фосфор и все другие элементы присутствуют в значительно меньших количествах.
Согласно графику кривой содержания (вверху справа), аргон, значительный, если не главный компонент атмосферы, вообще не появляется в коре. Это связано с тем, что атмосфера имеет гораздо меньшую массу, чем кора, поэтому аргон, остающийся в коре, мало влияет на ее массовую долю, в то время как в то же время накопление аргона в атмосфере стало достаточно большим, чтобы быть значительным.
Городские почвы
Полный список содержания элементов в городских почвах см. В разделе Содержание элементов (страница данных) # Городские почвы .
Источник