Самый распространённый элемент во вселенной
Безусловно, что в нашем понимании вселенная это нечто единое целое. Но имеющее свою структуру и состав. Сюда относятся все небесные тела и объекты, материя, энергия, газ, пыль и многое другое. Все это образовалось и существует, независимо от того, видим ли мы это или ощущаем.

Учёные давно рассматривают такие вопросы: Что же образовало такую вселенную? И какие элементы её наполняют?
Сегодня мы поговорим о том, какой элемент самый распространённый во вселенной.
Водород
Оказывается этот химический элемент самый лёгкий в мире. Кроме тго, его одноатомная форма составляет примерно 87% всего состава вселенной. Помимо того, он содержится в большинстве молекулярных соединений. Даже в воде, или, к примеру, он является частью органических веществ. Вдобавок водород выступает особенно важной составляющей частью кислотно-основных реакций.
Кроме того, элемент растворим в большинстве металлах. Что интересно, водород не обладает запахом, цветом и вкусом.

В процессе изучения, учёные называли водород горючим газом.
Как только не определяли его. В своё время он носил имя рождающий воду, а затем водотворное вещество.
Лишь в 1824 году ему присвоили название водород.
Во вселенной водород входит в состав 88,6% всех атомов. Остальное в большем количестве составляет гелий. И лишь малая часть это прочие элементы.
Следственно, звёзды и другие газы имеют в своём составе в основном водород.
Кстати, опять же он имеется и в звёздных температурах. Однако в виде плазмы. А в космическом пространстве он представлен в виде молекул, атомов и ионов. Интересно, что водород способен формировать молекулярные облака.

Характеристика водорода
Водород уникальный элемент, так как не имеет нейтрон. Он содержит лишь один протон и электрон.
Как указывалось, это самый лёгкий газ. Важно, что чем меньше масса молекул, тем выше их скорость. На это не влияет даже температура.
Теплопроводность водорода одна из высоких среди всех газов.
Помимо всего прочего, он хорошо растворим в металлах, что влияет на его способность диффундировать через них. Иногда процесс приводит к разрушению. К примеру, взаимодействие водорода и углерода. В этом случае происходит декарбонизация.
Появление водорода
Возник во вселенной после Большого взрыва. Как и все химические элементы. По теории, в первые микросекунды после взрыва температура вселенной была выше 100 млрд градусов. Что образовало связь трёх кварков. В свою очередь, эта взаимодействие создало протон. Таким образом, возникло ядро атома водорода. В процессе расширения температура упала, и кварки образовали протоны и нейтроны. Так, на самом деле, возник водород.

Гелий
В промежутке от 1 до 100 секунд после образования вселенной часть протонов и нейтронов соединилась. Тем самым образовав другой элемент-гелий.
В дальнейшем расширение пространства и как следствие снижение температуры приостановило соединительные реакции. Что важно, они вновь запустились внутри звёзд. Так образовались атомы других химических элементов.
В результате получается, что водород и гелий являются основными двигателями образования остальных элементов.

Гелий вообще является вторым по распространённости элементом во вселенной. Его доля составляет 11,3% всего космического пространства.
Свойства гелия
Он, так же как и водород, не имеет запаха, цвета и вкуса. Вдобавок, это второй по лёгкости газ. Но его температура кипения самая низкая из всех известных.
Гелий — это инертный, нетоксичный и одноатомный газ. Теплопроводность его высокая. По этой характеристике он вновь стоит на втором месте после водорода.
Добыча гелия осуществляется методом разделения при низкой температуре.
Интересно, что раньше гелий считали металлом. Но в процессе изучения определили, что это газ. При том, основной в составе вселенной.

Все элементы на Земле, за исключением водорода и гелия, породила миллиарды лет назад алхимия звезд, часть которых является ныне неприметными белыми карликами где-то на другой стороне Млечного Пути. Азот наших ДНК, кальций наших зубов, железо нашей крови, углерод наших яблочных пирогов созданы в недрах сжимающихся звезд.
Мы сотворены из звездного вещества.
Карл Саган
Применение элементов
Человечество научилось добывать и применять с пользой для себя химические элементы. Так водород и гелий применяют во многих сферах деятельности. Например в:
- пищевой промышленности;
- металлургии;
- химической промышленности;
- нефтепереработке;
- производстве электроники;
- косметической промышленности;
- геологии;
- даже в военной сфере и др.
Как видно, эти элементы играют важную роль в жизни вселенной. Очевидно, само наше существование напрямую зависит от них. Мы знаем, что ежеминутно происходит рост и движение вселенной. И несмотря на то, что они по отдельности небольшие, все вокруг основано из этих элементов.
Поистине, водород и гелий, также как другие химические элементы, уникальны и удивительны. Пожалуй с этим невозможно поспорить.
Источник
Сюрприз: угадайте, какой элемент во Вселенной на третьем месте по распространенности?
«Два самых распространенных элемента во Вселенной — водород и глупость». — Харлан Эллисон. После водорода и гелия, в периодической таблице сплошь и рядом идут сюрпризы. В числе самых удивительных фактов есть и то, что каждый материал, которого мы когда-либо касались, который видели, с которым взаимодействовали, состоит из одних и тех же двух вещей: атомных ядер, заряженных положительно, и электронов, заряженных отрицательно. То, как эти атомы взаимодействуют между собой — как они толкаются, связываются, притягиваются и отталкиваются, создавая новые стабильные молекулы, ионы, электронные энергетические состояния, — собственно, определяет живописность мира вокруг нас.
Даже если именно квантовые и электромагнитные свойства этих атомов и их составляющих позволяют нашей Вселенной существовать с теми свойствами, что у нее есть, важно понимать, что Вселенная начиналась вовсе не со всеми этими элементами. Совсем наоборот, начинала она практически без них.
Видите ли, чтобы достичь разнообразия структур связи и построить сложные молекулы, которые лежат в основе всего, что нам известно, нужно очень много атомов. Не в количественном выражении, а в разнообразном, то есть чтобы были атомы с разным числом протонов в их атомных ядрах: именно это делает элементы разными.
Наши тела нуждаются в таких элементах, как углерод, азот, кислород, фосфор, кальций и железо. Кора нашей Земли нуждается в таких элементах, как кремний и множество других тяжелых элементов, тогда как ядро Земли — чтобы вырабатывать тепло — нуждается в элементах, наверное, всей периодической таблицы, которые встречаются в природе: торий, радий, уран и даже плутоний.
Прошло некоторое время. Первые ядра слились вместе и больше не разошлись, произведя водород и его изотопы, гелий и его изотопы, а также крошечные едва различимые объемы лития и бериллия, последний впоследствии радиоактивно распался на литий. С этого началась Вселенная: по числу ядер — 92% водорода, 8% гелия и примерно 0,00000001% лития. По массе — 75-76% водорода, 24-25% гелия и 0,00000007% лития. В начале было два слова: водород и гелий, на этом, можно сказать, все.
Сотни тысяч лет спустя Вселенная остыла достаточно, чтобы смогли образоваться нейтральные атомы, а десятки миллионов лет спустя гравитационный коллапс позволил состояться первым звездам. Вместе с этим, явление ядерного синтеза не только наполнило светом Вселенную, но и позволило сформироваться тяжелым элементам.
К моменту рождения первой звезды, где-то 50-100 миллионов лет после Большого Взрыва, обильное количество водорода начало сливаться в гелий. Но что еще более важно, самые массивные звезды (в 8 раз массивнее нашего Солнца) сжигали свое топливо очень быстро, выгорая всего за пару лет. Как только в ядрах таких звезд заканчивался водород, гелиевое ядро сжималось и начинало сливать три ядра атома в углерод. Потребовался всего триллион этих тяжелых звезд в ранней Вселенной (которая образовала намного больше звезд в первые несколько сотен миллионов лет), чтобы литий был побежден.
И тут вы, наверное, думаете, что углерод стал элементом номер три в наши дни? Об этом можно подумать, поскольку звезды синтезируют элементы послойно, как луковица. Гелий синтезируется в углерод, углерод в кислород (позже и при большей температуре), кислород в кремний и серу, а кремний в железо. В конце цепочки железо не может слиться больше ни во что, поэтому ядро взрывается и звезда становится сверхновой.
- медленного захвата нейтрона (s-процесс), последовательно выстраивающего элементы;
- слияния ядер гелия с тяжелыми элементами (с образованием неона, магния, аргона, кальция и так далее);
- быстрого захвата нейтрона (r-процесс) с образованием элементов до урана и дальше.
Но у нас было не одно поколение звезд: у нас было много таких, и поколение, которое существует ныне, построено в первую очередь не на девственном водороде и гелии, но и на остатках от предыдущих поколений. Это важно, поскольку без этого у нас никогда бы не было твердых планет, лишь газовые гиганты из водорода и гелия, исключительно.
За миллиарды лет процесс образования и смерти звезд повторялся, все с более и более обогащенными элементами. Вместо того чтобы просто сливать водород в гелий, массивные звезды сливают водород в цикле C-N-O, со временем выравнивая объемы углерода и кислорода (и чуть меньше азота).
Кроме того, когда звезды проходят через гелиевый синтез с образованием углерода, довольно просто захватить лишний атом гелия с образованием кислорода (и даже добавить еще один гелий к кислороду с образованием неона), и даже наше Солнце будет делать это во время фазы красного гиганта.
Когда мы смотрим на останки сверхновой и планетарные туманности — остатки очень массивных звезд и солнцеподобных звезд соответственно — мы находим, что кислород превосходит углерод массово и количественно в каждом из случаев. Мы также обнаружили, что ни один из других элементов тяжелее и близко не стоит.
Что будущее нам готовит?
Вселенная меняется. Кислород — третий по распространенности элемент в современной Вселенной, и в очень, очень далеком будущем, возможно, поднимется выше водорода. Каждый раз, когда вы вдыхаете воздух и чувствуете удовлетворение от этого процесса, помните: звезды — единственная причина существования кислорода.
Источник
Самые распространенные химические элементы на Земле и во Вселенной
По мнению большинства ученых, возникновение химических элементов во вселенной произошло после Большого Взрыва. При этом, каких-то веществ образовалось больше, каких-то меньше. В нашем топе представлен список самых распространенных химических элементов на Земле и во вселенной.
Водород
Лидером рейтинга становится водород. В таблице Менделеева он обозначен символом H и атомным номером 1. Открыт в 1766 году Г. Кавендишем. А еще через 15 лет этот же ученый выяснил, что водород участвует в образовании большинства веществ на планете.
Водород не только наиболее распространенный, но и самый взрывной и легкий химический элемент во вселенной в природе. В земной коре его объем равен 1%, но количество атомов – 16%. Данный элемент входит во множество природных соединений, например, в нефть, природный газ, уголь.
В свободном состоянии водород практически не встречается. На поверхности Земли присутствует в некоторых вулканических газах. В воздухе он есть, но в очень малых дозах. Водородом занято почти половина строения звезд, большая часть межзвездной сферы и газов туманностей.
Гелий
Второе место среди наиболее распространенных элементов во вселенной занимает гелий. Он же считается вторым по легкости. Кроме того, у гелия самая низкая температура кипения среди всех известных веществ.
Открыт в 1868 году французским астрономом П. Жансеном, обнаружившим яркую желтую линию в околосолнечной атмосфере. А в 1895 году английский химик У. Рамзай доказал существование этого элемента на Земле.
За исключением экстремальных условий, гелий представлен только в виде газа. В космосе он был образован в первые мгновения после Большого взрыва. Сегодня гелий появляется при термоядерном синтезе с водородом в звездных глубинах. На Земле образуется после распада тяжелых элементов.
Кислород
Самым распространенным элементом в земной коре (49,4%) является кислород. Обозначается символом O и номером 8. Незаменим для существования человека.
Кислород – химически неактивный неметалл. При стандартных условиях находится в бесцветном газообразном состоянии, без вкуса и запаха. Молекула включает два атома. В жидком виде отличается светло-голубым оттенком, в твердом выглядит как как кристаллы с синеватым отливом.
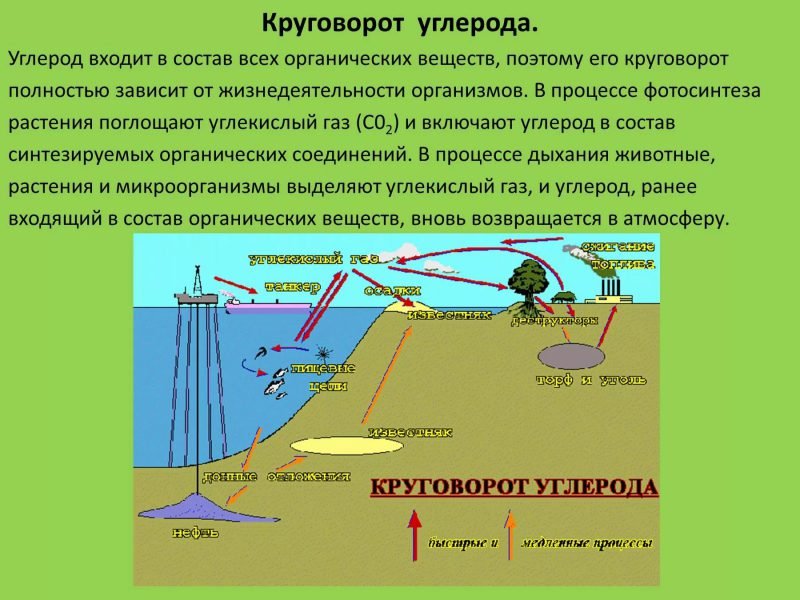
Кислород необходим всем живым существам на Земле. Он участвует в круговороте веществ свыше 3 млрд лет. Играет значимую роль в хозяйстве и природе:
- Участвует в фотосинтезе растений;
- Поглощается живыми организмами при дыхании;
- Выступает в роли окислителя в процессах брожения, гниения, ржавления;
- Содержится в органических молекулах;
- Необходим для получения ценных веществ органического синтеза.
В сжиженном состоянии кислород применяют для резки и сварки металлов, подземных и подводных работ, действий на большой высоте в безвоздушном пространстве. Кислородные подушки незаменимы при выполнении лечебных манипуляций.
На 4 месте азот – двухатомный бесцветный и безвкусный газ. Существует не только на нашей, но и на нескольких других планетах. Из него состоит почти 80% земной атмосферы. Даже человеческое тело содержит до 3% данного элемента.
Помимо газообразного, существует жидкий азот. Он широко используется в строительстве, промышленности, лечебном деле. Его применяют при охлаждении техники, заморозке органики, избавления от бородавок. В жидком виде азот не взрывоопасен и не токсичен.
Элемент блокирует окисление и гниение. Широко применяется в шахтах для формирование взрывобезопасной среды. В химическом производстве с его помощью создают аммиак, удобрения, красители, в кулинарии используют как хладагент.
Неон – это инертный и бесцветный атомный газ без запаха. Открыт в 1989 году англичанами У. Рамзаем и М. Траверсом. Выведен из разжиженного воздуха путем исключения других элементов.
Название газа переводится как «новый». Во Вселенной распределен крайне неравномерно. Максимальная концентрация выявлена на горячих звездах, в воздухе внешних планет нашей системы и в газовых туманностях.
На Земле неон в основном содержится в атмосфере, в других частях его ничтожно мало. Объясняя неоновую скудность нашей планеты, ученые выдвинули гипотезу, что когда-то земной шар лишился своей первичной атмосферы, а вместе с ней и основного объема инертных газов.
Углерод
На 6 месте в списке самых распространенных химических элементов на Земле находится углерод. В таблице Менделеева обозначен буквой C. Обладает необычайными свойствами. Является ведущим биогенным элементом планеты.
Известен с давних времен. Входит в структуру каменного угля, графита, алмазов. Содержание в земной тверди – 0,15%. Не слишком большая концентрация объясняется тем, что в природе углерод подвергается постоянной циркуляции.
Существует несколько минералов, содержащих данный элемент:
- Антрацит;
- Нефть;
- Доломит;
- Известняк;
- Горючий сланец;
- Торф;
- Бурый и каменный уголь;
- Природный газ;
- Битум.
Хранилищем углеродных групп являются живые существа, растения и воздух.
Кремний
Кремний – неметалл, часто встречающийся в земной коре. В свободном виде выведен в 1811 году Ж. Тенаром и Ж. Гей-Люссаком. Содержание в планетной оболочке – 27,6-29,5% по массе, в океанической воде – 3 мг/л.
О множестве соединений кремния было известно еще в древние времена. Но чистый элемент долго оставался за гранью человеческих познаний. Самыми популярными соединениями были поделочные и драгоценные камни на базе оксида кремния:
В природе элемент содержится в:
- Горных массивных породах и залежах;
- Растениях и морских жителях;
- Глубоко в почве;
- В организмах живых существ;
- В низу водоемов.
Кремний играет огромную роль в формировании человеческого организма. Ежедневно внутрь должно попадать минимум 1 грамм элемента, иначе начнут появляться неприятные недуги. Тоже самое можно сказать про растения и животных.
Магний
Магний – ковкий, легкий металл серебристого оттенка. В таблице Менделеева отмечен символом Mg. Получен в 1808 году англичанином Г. Дэви. Занимает 8 место по объему в земной коре. Природными источниками являются минеральные отложения, рассолы и морская вода.
В стандартном состоянии покрыт слоем оксида магния, который распадается при температуре +600-650 0 C. При сгорании выделяет ярко-белое пламя с формированием нитрида и оксида.
Металлический магний используется во многих сферах:
- При регенерации титана;
- В получении легких литейных сплавов;
- В создании зажигательных и осветительных ракет.
Магниевые сплавы – важнейший конструкционный материал в транспортной и авиационной промышленности.
Магний не зря называют «металлом жизни». Без него невозможно большинство физиологических процессов. Он играет ведущую роль в функционировании нервной и мышечной ткани, участвует в липидном, белковом и углеводном обмене.
Железо
Железо – это ковкий серебристо-белый металл с высоким уровнем химической реакции. Обозначается буквами Fe. Быстро ржавеет при повышенных температурах/влажности. Воспламеняется в очищенном кислороде. Способен самовозгораться в мелкодисперном воздухе.
В обиходе железом именуют его сплавы с минимальным объемом добавок, сохраняющие податливость чистого металла:
Есть мнение, что железо составляет основной процент земного ядра. Имеет несколько уровней окисления, что является важнейшей геохимической чертой.
Десятое место в списке самых распространенных химических элементов на Земле занимает сера. Обозначается буквой S. Проявляет неметаллические характеристики. В самородном состоянии выглядит как светло-желтый порошок с характерным ароматом либо блестящие кристаллы стеклянно-желтого цвета. В регионах древнего и новейшего вулканизма встречаются рассыпчатые залежи серы.
Без серы невозможно проведения многих промышленных операций:
- Выпуск препаратов для сельскохозяйственных нужд;
- Придание особых характеристик некоторым сортам стали;
- Образование серной кислоты;
- Выработка резины;
- Производство сульфатов и другое.
Медицинская сера содержится в кожных мазях, ею лечат ревматизм и подагру, включают в состав косметических препаратов по уходу за кожей. Она применяется в изготовлении гипса, слабительных лекарств и средств от гипертонии.
Видео
Источник