Какого металла больше всего во Вселенной
Самым распространенным химическим элементом на нашей планете является углерод. Но в масштабах Вселенной Земля — лишь песчинка среди бескрайнего моря звезд и галактик. И в связи с этим становится интересным, а из чего состоит наша Вселенная? Что является основой далеких планет и астероидов? Какой элемент периодической таблицы самый главный?
Самый распространенный химический элемент во Вселенной
Если говорить о том, какой элемент самый распространенный во Вселенной, то тут все будет очень просто. На первом месте идет водород, затем гелий, кислород, неон и замыкает пятерку лидеров железо. А теперь давайте подумаем, какой элемент выбивается из общей картины.
Правильно! Железо! Почему? Да потому, что все остальные представители таблицы Менделеева, кроме железа, являются газами. А железо — это металл. Таким образом железо — это самый распространенный металл во всей Вселенной. При этом он и один из самых важных, ведь если газы формируют в основном атмосферу небесных тел, то железо является основой планет. А значит можно сказать, что если бы не было железа, то не было бы и большинства объектов во Вселенной.
Как ученые определили, что железо — самый распространенный металл во Вселенной
По сообщению журнала The Astrophysical Journal, группа астрохимиков из США пришла к такому выводу, рассчитав спектр поглощения кластеров железа. То есть ученые провели спектральный анализ удаленных объектов. Если не вдаваться в подробности, то объяснить это можно следующим образом.
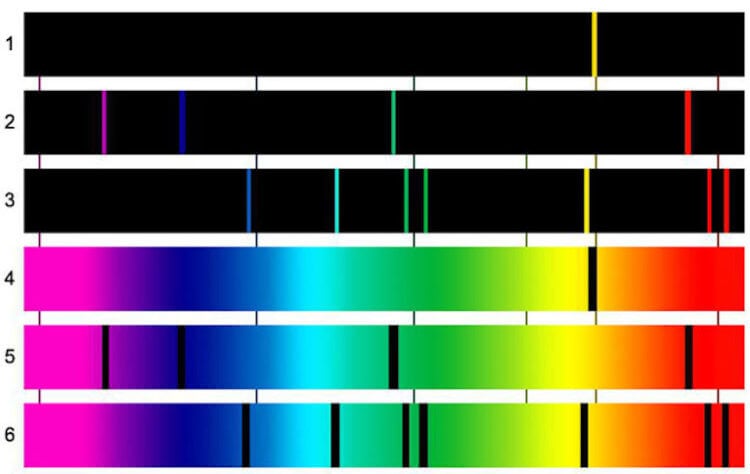
Когда мы что-либо видим, это означает, что от этого объекта отражается свет и мы улавливаем эти световые волны. Свет – это смесь электромагнитных колебаний, и каждое колебание имеет свою длину волны, и, соответственно, свой цвет. Есть 7 основных цветов, а также оттенков и переходов между ними. Когда проводится спектральный анализ, изучается именно то, как химические элементы поглащают или отражают свет. В итоге получается спектрограмма. На основе получившейся картины можно сделать вывод о характеристиках испустившего свет объекта. Простой пример — радуга после дождя. Капли дождя разделяют свет, исходящий от Солнца.
Где находится «космическое железо»
Большая часть железа Вселенной сконцентрирована внутри планет и в межзвездном газе. Кроме того, как показывает новое исследование, не мало железа находится в связи с углеродом, формируя особые молекулы, называемые полиинами. При этом ранее предполагалось, что эти самые полиины — это соединения углерода без примесей железа.
«Атомы железа объединяются в особые соединения с углеродом и основная проблема в том, что эти соединения имеют почти такой же спектр, что и чистые углеводороды. Поэтому ранее мы могли легко их проглядеть», — говорит ведущий автор исследования Фрэнк Тиммес
Хотите узнать что-то новое? Подписывайтесь на наш канал в Яндекс.Дзен. Там регулярно выходят материалы, которых не найти на сайте.
Источник
Самый распространённый элемент во вселенной
Безусловно, что в нашем понимании вселенная это нечто единое целое. Но имеющее свою структуру и состав. Сюда относятся все небесные тела и объекты, материя, энергия, газ, пыль и многое другое. Все это образовалось и существует, независимо от того, видим ли мы это или ощущаем.

Учёные давно рассматривают такие вопросы: Что же образовало такую вселенную? И какие элементы её наполняют?
Сегодня мы поговорим о том, какой элемент самый распространённый во вселенной.
Водород
Оказывается этот химический элемент самый лёгкий в мире. Кроме тго, его одноатомная форма составляет примерно 87% всего состава вселенной. Помимо того, он содержится в большинстве молекулярных соединений. Даже в воде, или, к примеру, он является частью органических веществ. Вдобавок водород выступает особенно важной составляющей частью кислотно-основных реакций.
Кроме того, элемент растворим в большинстве металлах. Что интересно, водород не обладает запахом, цветом и вкусом.

В процессе изучения, учёные называли водород горючим газом.
Как только не определяли его. В своё время он носил имя рождающий воду, а затем водотворное вещество.
Лишь в 1824 году ему присвоили название водород.
Во вселенной водород входит в состав 88,6% всех атомов. Остальное в большем количестве составляет гелий. И лишь малая часть это прочие элементы.
Следственно, звёзды и другие газы имеют в своём составе в основном водород.
Кстати, опять же он имеется и в звёздных температурах. Однако в виде плазмы. А в космическом пространстве он представлен в виде молекул, атомов и ионов. Интересно, что водород способен формировать молекулярные облака.

Характеристика водорода
Водород уникальный элемент, так как не имеет нейтрон. Он содержит лишь один протон и электрон.
Как указывалось, это самый лёгкий газ. Важно, что чем меньше масса молекул, тем выше их скорость. На это не влияет даже температура.
Теплопроводность водорода одна из высоких среди всех газов.
Помимо всего прочего, он хорошо растворим в металлах, что влияет на его способность диффундировать через них. Иногда процесс приводит к разрушению. К примеру, взаимодействие водорода и углерода. В этом случае происходит декарбонизация.
Появление водорода
Возник во вселенной после Большого взрыва. Как и все химические элементы. По теории, в первые микросекунды после взрыва температура вселенной была выше 100 млрд градусов. Что образовало связь трёх кварков. В свою очередь, эта взаимодействие создало протон. Таким образом, возникло ядро атома водорода. В процессе расширения температура упала, и кварки образовали протоны и нейтроны. Так, на самом деле, возник водород.

Гелий
В промежутке от 1 до 100 секунд после образования вселенной часть протонов и нейтронов соединилась. Тем самым образовав другой элемент-гелий.
В дальнейшем расширение пространства и как следствие снижение температуры приостановило соединительные реакции. Что важно, они вновь запустились внутри звёзд. Так образовались атомы других химических элементов.
В результате получается, что водород и гелий являются основными двигателями образования остальных элементов.

Гелий вообще является вторым по распространённости элементом во вселенной. Его доля составляет 11,3% всего космического пространства.
Свойства гелия
Он, так же как и водород, не имеет запаха, цвета и вкуса. Вдобавок, это второй по лёгкости газ. Но его температура кипения самая низкая из всех известных.
Гелий — это инертный, нетоксичный и одноатомный газ. Теплопроводность его высокая. По этой характеристике он вновь стоит на втором месте после водорода.
Добыча гелия осуществляется методом разделения при низкой температуре.
Интересно, что раньше гелий считали металлом. Но в процессе изучения определили, что это газ. При том, основной в составе вселенной.

Все элементы на Земле, за исключением водорода и гелия, породила миллиарды лет назад алхимия звезд, часть которых является ныне неприметными белыми карликами где-то на другой стороне Млечного Пути. Азот наших ДНК, кальций наших зубов, железо нашей крови, углерод наших яблочных пирогов созданы в недрах сжимающихся звезд.
Мы сотворены из звездного вещества.
Карл Саган
Применение элементов
Человечество научилось добывать и применять с пользой для себя химические элементы. Так водород и гелий применяют во многих сферах деятельности. Например в:
- пищевой промышленности;
- металлургии;
- химической промышленности;
- нефтепереработке;
- производстве электроники;
- косметической промышленности;
- геологии;
- даже в военной сфере и др.
Как видно, эти элементы играют важную роль в жизни вселенной. Очевидно, само наше существование напрямую зависит от них. Мы знаем, что ежеминутно происходит рост и движение вселенной. И несмотря на то, что они по отдельности небольшие, все вокруг основано из этих элементов.
Поистине, водород и гелий, также как другие химические элементы, уникальны и удивительны. Пожалуй с этим невозможно поспорить.
Источник
Топ-10: самые распространенные химические элементы во всей Вселенной
Все мы знаем, что водород наполняет нашу Вселенную на 75%. Но знаете ли вы, какие еще есть химические элементы, не менее важные для нашего существования и играющие значительную роль для жизни людей, животных, растений и всей нашей Земли? Элементы из этого рейтинга формируют всю нашу Вселенную!
10. Сера (распространенность относительно кремния – 0.38)

Этот химический элемент в таблице Менделеева значится под символом S и характеризуется атомным номером 16. Сера очень распространена в природе.
9. Железо (распространенность относительно кремния – 0.6)
Обозначается символом Fe, атомный номер – 26. Железо очень часто встречается в природе, особенно важную роль оно играет в формировании внутренней и внешней оболочки ядра Земли.
8. Магний (распространенность относительно кремния – 0.91)

В таблице Менделеева магний можно найти под символом Mg, и его атомный номер – 12. Что самое удивительное в этом химическом элементе, так это то, что он чаще всего выделяется при взрыве звезд в процессе их преобразования в сверхновые тела.
7. Кремний (распространенность относительно кремния – 1)

Обозначается как Si. Атомный номер кремния – 14. Этот серо-голубой металлоид очень редко встречается в земной коре в чистом виде, но довольно распространен в составе других веществ. Например, его можно обнаружить даже в растениях.
6. Углерод (распространенность относительно кремния – 3.5)
Углерод в таблице химических элементов Менделеева значится под символом С, его атомный номер – 6. Самой знаменитой аллотропной модификацией углерода являются одни из самых желанных драгоценных камней в мире – алмазы. Углерод активно применяют и в других в промышленных целях более будничного назначения.
5. Азот (распространенность относительно кремния – 6.6)

Символ N, атомный номер 7. Впервые открытый шотландским врачом Дэниелом Рутерфордом (Daniel Rutherford), азот чаще всего встречается в форме азотной кислоты и нитратов.
4. Неон (распространенность относительно кремния – 8.6)
Обозначается символом Ne, атомный номер — 10. Не секрет, что именно этот химический элемент ассоциируется с красивым свечением.
3. Кислород (распространенность относительно кремния – 22)

Химический элемент под символом О и с атомным номером 8, кислород незаменим для нашего существования! Но это не значит, что он присутствует только на Земле и служит только для человеческих легких. Вселенная полна сюрпризов.
2. Гелий (распространенность относительно кремния – 3.100)

Символ гелия – He, атомный номер – 2. Он бесцветен, не имеет запаха и вкуса, не ядовит, и его точка кипения – самая низкая среди всех химических элементов. А еще благодаря ему шарики взмывают ввысь!
1. Водород (распространенность относительно кремния – 40.000)
Истинный номер один в нашем списке, водород находится в таблице Менделеева под символом Н и обладает атомным номером 1. Это самый легкий химический элемент периодической таблицы и самый распространенный элемент во всей изученной человеком Вселенной.
Источник
Алюминий как химический элемент таблицы Менделеева
Как был открыт Алюминий
История такого химического элемента как алюминий напрямую связано с использованием так называемых «квасцов». Квасцы представляют собой алюминиевую соль, записи о которых впервые были обнаружены еще в V веке до нашей эры. Об этом химическом соединении алюминия впервые сделал заметки греческий историк Геродот. В те времена этот минерал был довольно популярен. Его в своей основе использовали в качестве красящего вещества, но природа его оставалась неизвестной. В 15 веках его широко использовали в текстильной промышленности. На сегодняшний день точно неизвестно когда начались попытки выделить чистый алюминий. Известно, что в 1754 году немецкий химик Андреас Сигизмунд Маргграф получил из «квасцов» так называемый «глинозем», который стал началом истории открытия алюминия.
Первые попытки производства металлического алюминия датируются 1760 годом. В 1782 году Антуан Лавуазье заподозрил, что «глинозем» полученный Маргграфом является оксидом нового химического элемента. Еще до получения нового химического элемента в 1807 Хэмфри Дэви предложил название aluminium, которое закрепилось и по сегодняшний день. Получить чистый аллюминий удалось только в 1824 году датскиму физику и химику Хансу Кристиану Эрстеду. Он проводил опыты над безводным хлоридом алюминия с амальгамой калия. В результате химической реакции образовался металлический порошок, который сегодня известен как алюминий. Более чистый алюминий был получен в 1827 году немецким химиком Фридрихом Веллером. Он использовал тот же метод что и Эрстед, но использовал металлический калий в качестве восстановителя.
Где и как добывают Алюминий
На сегодняшний день добыча алюминия является очень энергоемким процессом. Производство большей части алюминия осуществляется методом очистки бокситов. Боксит представляет собой алюминиевую руду состоящую из оксидов алюминия, железа, кремния — сырья для получения глинозема. Содержание промышленного глинозема в бокситах составляет от 40 до 60 процентов.
Первый промышленный метод крупномасштабного производства алюминия был открыт в 1886 году. В этом году французский инженер Пол Эрульт и американский химик Мартин Холл (отдельно друг от друга) разработали новый метод электролиза для получения алюминия. Сегодня этот метод известен в научном окружении как метод Холла–Эрульта. Этот процесс заключается в переработке глинозема в алюминий. Чуть позже, а именно в 1889 году, австрийский химик Карл Джозеф Байер открыл способ очистки боксита для получения глинозема. Этот метод сейчас известен как метод Байера. Современное производство алюминия основывается на извлечении глинозема из бокситов методом Байера и дальнейшей переработкой его в алюминий методом Холла–Эрульта.
Так как выплавка алюминия является очень энергозатратным производством заводы производители размещают в местах где есть недорогое электричество или имеется поддержка государства. Главными производителями алюминия в мире являются Китай, Россия, Индия, Канада и ОАЭ. При всем этом Китай производит больше 65% от всего алюминия производимого в мире. Годовой выход алюминия из Китая составляет около 32 000 тонн. В то время как Россия производит около 3500 тонн в год. Цена за тонну алюминия составляет около 2300$ США.
Распространенность Алюминия
Алюминий является довольно распространенным элементом как во Вселенной так и на Земле. В солнечной системе содержание алюминия составляет 3,15 частей на миллион. Он является 12 по распространенности елементом из всех известных и 3 из элементов с нечетными номерами после водорода и азота. Единственный стабильный изотоп алюминия с атомной массой 27 является восемнадцатым по распространенности ядром во Вселенной. Он создается почти сразу после слияния водорода в массивных звездах, которые затем преобразуются в сверхновые второго типа.
На Земле алюминий так же является довольно распространенным элементом. Соотношение его частей на Земле на порядок выше чем во Вселенной. От общей массы Земли масса алюминия составляет около 1.6%. Это делает этот химический элемент седьмым по распространенности на Земле из всех и первым среди металлов. Что же касается земной коры то аллюминий занимает почетное 3 место после кислорода и кремния. Соответственно он так же является самым распространенным металлом с процентом от общей массы в 8.3%, что согласитесь в масштабах нашей планеты немало. В земной коре большое количество силикатов содержит алюминий. В тоже время в мантии Земли алюминия содержится всего 2.38%, что значительно меньше в отношении земной коры.
Применение Алюминия
Алюминий является очень широкоприменяемым цветным металлом. Ежегодное производство алюминия составляет около 60 млн тонн. Он занимает второе место по производству среди металлов после железа. Основными областями применения алюминия являются машиностроение и транспорт, строительство, упаковка и электрика, а так же в различных бытовых приборах, медицина и ветеринария. Вообще нашу повседневную жизнь сложно представить без алюминия. Конечно он применяется не в чистом виде, а в качестве сплавов и соединений.
В современных легковых автомобилях около 20% частей состоят из алюминиевых сплавов. В электротехнике проводниковые элементы, трансформаторы, конденсаторы изготавливаются с применением алюминия. Что же касается упаковочной структуры, то тут можно отметить алюминиевую фольгу, алюминиевые банки из под напитков. Если брать строительство, то тут каркасы, кровля, сайдинг, различного рода заклепки. Алюминий используется в случаях когда важны легкость, корозийная прочность и многие другие техгические характеристики. Многие бытовые предметы имеют в своем составе алюминий, который обеспечивает пригодный внешний вид и заданые характеристики предметов. Фосфат алюминия применяется при изготовлении целлюлозы, бумаги, лаков красок, стекла, керамики и многого другого.
Подведя итог стоит заметить, что из-за низкой стоимости алюминия и физических свойств его применение очень широко и разнообразно почти во всех сферах жизнедеятельности человека.
Интересные факты
Интересных фактов связанных с алюминием очень много. Стоит начать с того, что в период от его открытия и до начала ено масштабного производства, был период времени когда алюминий стоил дороже золота. Даже в 1900 году стоимость тонны алюминия оценивалась в 14000$ в то время как сейчас его стоимость около 2300$ за тонну. Стоит отметить еще и дороговизну электроэнергии для изготовления этого металла. Стоимость затраченного электричества для изготовления алюминия составляет от 20 до 40% от стоимости металла. В США к примеру для изготовления этого материала используется 5% от общего количества электроэнергии.
Стоит заметить еще и то что ионы алюминия в значительных количествах содержатся в продуктах питания. Согласно исследованию ученых, взрослый европеец ежедневно вместе с пищей потребляет до 13 мг алюминия. Европейский орган по безопасности пищевых продуктов задает максимальную недельную дозу для человека 1 мг на 1 кг веса. Вообще, вопрос токсичности алюминия для организма человека является очень спорным. Сейчас ученые спорят о причастности ионов алюминия к таким болезням как Альцгеймер и Паркинсон.
Что же касается воздействия на живую природу, то тут можно заметить тот факт, что ионы алюминия снижают скорость роста растений в кислых почвах. Этот химический элемент в небольших количествах содержится в воздухе и вместе с осадками способен выпадать на землю. Наибольшее количество алюминия в воздухе обнаруживается возле мест добычи, угольных шахт и электростанций. Осадки в таких местах называются кислотными из-за химических реакций алюминия и могут оказывать пагубное воздействие на человека.
Источник