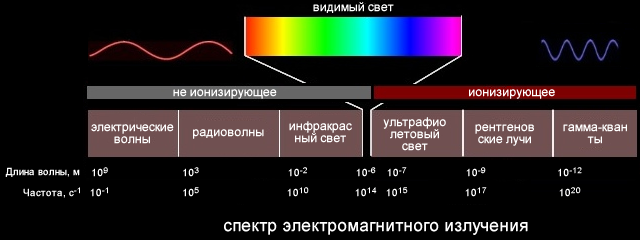
Спектр солнца это сплошной спектр
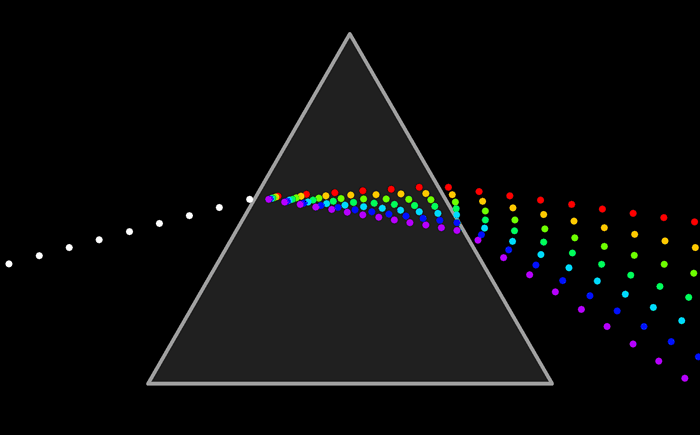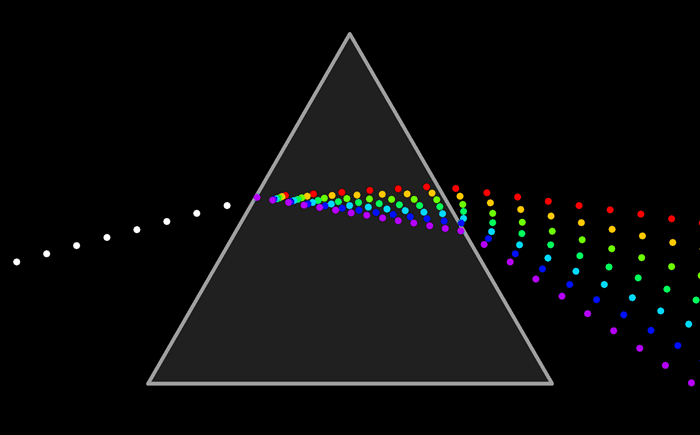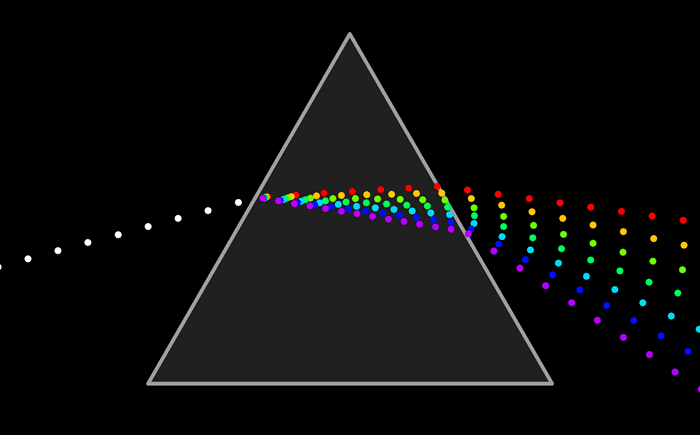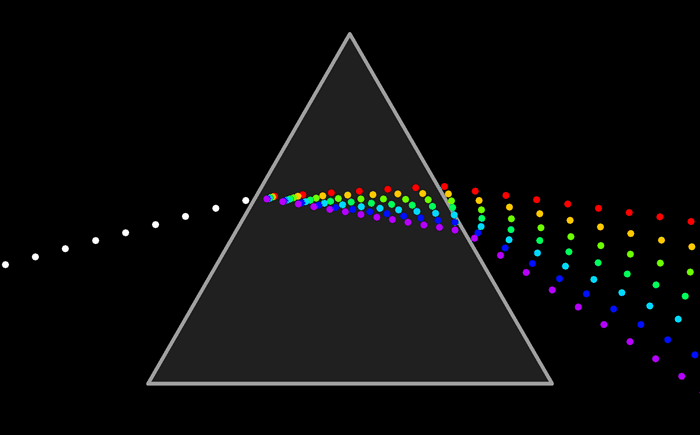
Ни один из источников не дает монохроматического света, т.е. света строго определенной длины волны. В этом можно убедиться на опытах по разложению света в спектр с помощью призмы, а также опыты по интерференции и дифракции.
Та энергия, которую несет с собой свет от источника, определенным образом распределена по волнам всех длин, входящим в состав светового пучка.
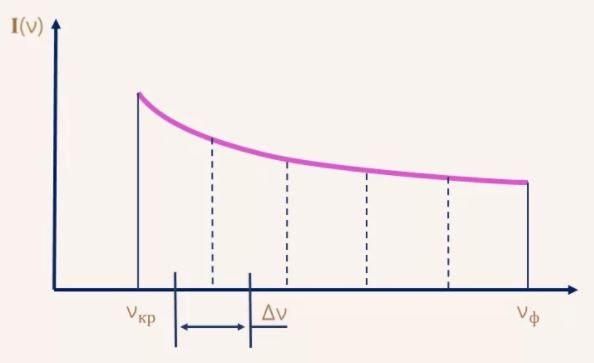
Для характеристики распределения излучения по частотам нужно ввести новую величину: интенсивность, приходящуюся на единичный интервал частот. Эту величину называют спектральной плотностью интенсивности излучения.
Спектральную плотность потока излучения можно найти экспериментально. Для этого надо с помощью призмы получить спектр излучения, например, электрической дуги, и измерить плотность потока излучения, приходящегося на небольшие спектральные интервалы шириной Δν.
Полагаться на глаз при оценке распределения энергии нельзя. Глаз обладает избирательной чувствительностью к свету: максимум его чувствительности лежит в желто-зеленой области спектра. Лучше всего воспользоваться свойством черного тела почти полностью поглощать свет всех длин волн. При этом энергия излучения (т.е. света) вызывает нагревание тела. Поэтому достаточно измерить температуру тела и по ней судить о количестве поглощенной в единицу времени энергии.
Спектры излучения
Спектральный состав излучения атомов различных веществ весьма разнообразен. Тем не менее, все спектры можно разделить на три сильно отличающихся друг от друга типа.
Сплошной (непрерывный) спектр
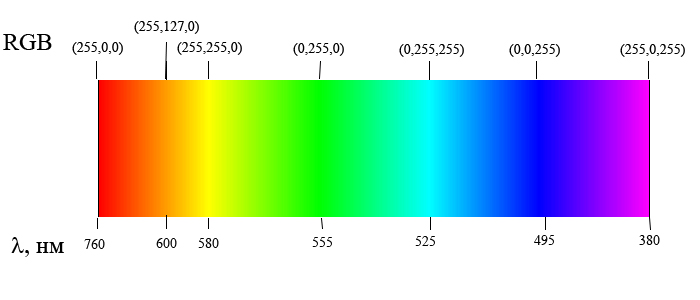
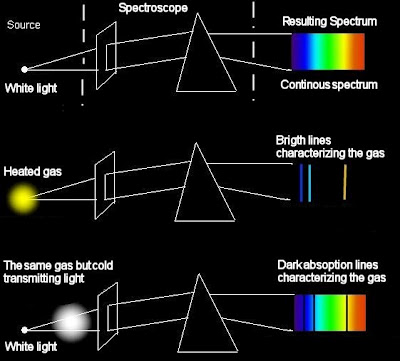
Накаленные твердые и жидкие тела и газы (при большом давлении) испускают свет, разложение которого дает сплошной спектр, в котором спектральные цвета непрерывно переходят один в другой. Характер непрерывного спектра и сам факт его существования определяются не только свойствами отдельных излучающих атомов, но и взаимодействием атомов друг с другом. Сплошные спектры одинаковы для разных веществ, и поэтому их нельзя использовать для определения состава вещества.
Линейчатый (атомный) спектр
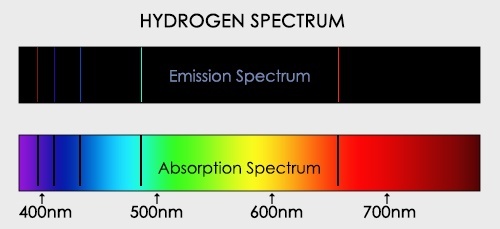
Возбужденные атомы разреженных газов или паров испускают свет, разложение которого дает линейчатый спектр,состоящий из отдельных цветных линий. Каждый химический элемент имеет характерный для него линейчатый спектр. Атомы таких веществ не взаимодействуют друг с другом и излучают свет только определенных длин волн. Изолированные атомы данного химического элемента излучают строго определенные длины волн. Это позволяет по спектральным линиям судить о химическом составе источника света.
Обычно для наблюдения линейчатых спектров используют свечение паров вещества в пламени или свечение газового разряда в трубке, наполненной исследуемым газом. При увеличении плотности атомарного газа отдельные спектральные линии расширяются и, при очень большой плотности газа, когда взаимодействие атомов становится существенным, эти линии перекрывают друг друга, образуя непрерывный спектр.
Молекулярный (полосатый) спектр
Спектр молекулы состоит из большого числа отдельных линий, сливающихся в полосы, четкие с одного края и размытые с другого. В отличие от линейчатых спектров полосатые спектры создаются не атомами, а молекулами, не связанными или слабо связанными друг с другом. Серии очень близких линий группируются на отдельных участках спектра и заполняют целые полосы.
 |
| Спектр угольной дуги (полосы молекул CN и C2) |
 |
| Спектр испускания паров молекулы йода |
 |
| Спектр молекулы Н2 |
В 1860 г. немецкие ученые Г. Кирхгоф и Р. Бунзен, изучая спектры металлов, установили следующие факты:
1) каждый металл имеет свой спектр;
2) спектр каждого металла строго постоянен;
3) введение в пламя горелки любой соли одного и того же металла всегда приводит к появлению одинакового спектра;
4) при внесении в пламя смеси солей нескольких металлов в спектре одновременно появляются все их линии;
5) яркость спектральных линий зависит от концентрации элемента в данном веществе.
Спектры поглощения
Если белый свет от источника, дающей сплошной спектр, пропускается через пары исследуемого вещества и затем разлагается в спектр, то на фоне сплошного спектра наблюдаются темные линии поглощения в тех же сам ых местах, где находились бы линии спектра испускания паров исследуемого элемента. Такие спектры получили название атомных спектров поглощения.
Все вещества, атомы которых находятся в возбужденном состоянии, излучают световые волны, энергия которых определенным образом распределена по длинам волн. Поглощение света веществом также зависит от длины волны. Атомы поглощают излучение лишь тех длин волн, которые они могут испускать при данной температуре.
Спектральный анализ
Спектральным анализом называется метод изучения химического состава вещества, основанный на исследовании его спектров. Отдельные линии в спектрах различных элементов могут совпадать, но в целом спектр каждого элемента является его индивидуальной характеристикой.
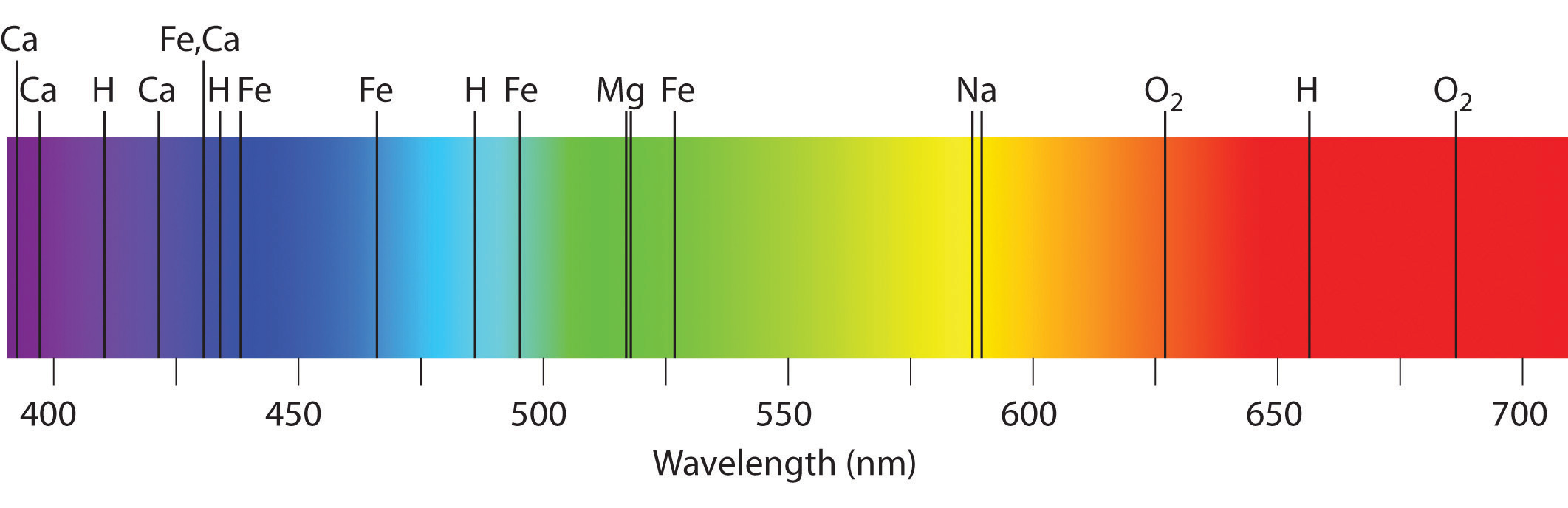
Спектральный анализ сыграл большую роль в науке. Например, в спектре Солнца (1814) были открыты фраунгоферовы темные линии, происхождение которых объясняется следующим образом. Солнце, являясь раскаленным газовым шаром (Т
6000 °С), испускает сплошной спектр. Солнечные лучи проходят через атмосферу Солнца (солнечную корону, температура которой
2000— 3000 °С. Корона поглощает из сплошного спектра излучение определенной частоты, а на Земле регистрируется солнечный спектр поглощения, по которому можно определить, какие химические элементы присутствуют в короне Солнца. По спектрам поглощения на Солнце были обнаружены все земные элементы, а также неизвестный ранее элемент, который назвали гелий. Через 26 лет (1894) открыли гелий на Земле. Благодаря спектральному анализу на Земле было открыто еще 25 химических элементов.
Фраунгоферовы линии дают информацию не только о химическом составе звезды, но и о ее температуре и давлении на поверхности. Более того, спектральный анализ Солнца и звезд показал, что входящие в их состав химические элементы имеются и на Земле, т.е. вещество Вселенной состоит из одного и того же набора элементов.
Спектральные аппараты
Спектроскопом называется прибор, с помощью которого визуально исследуется спектральный состав света, испускаемого некоторым источником. Если регистрация спектра происходит на фотопластинке, то прибор называется спектрографом.
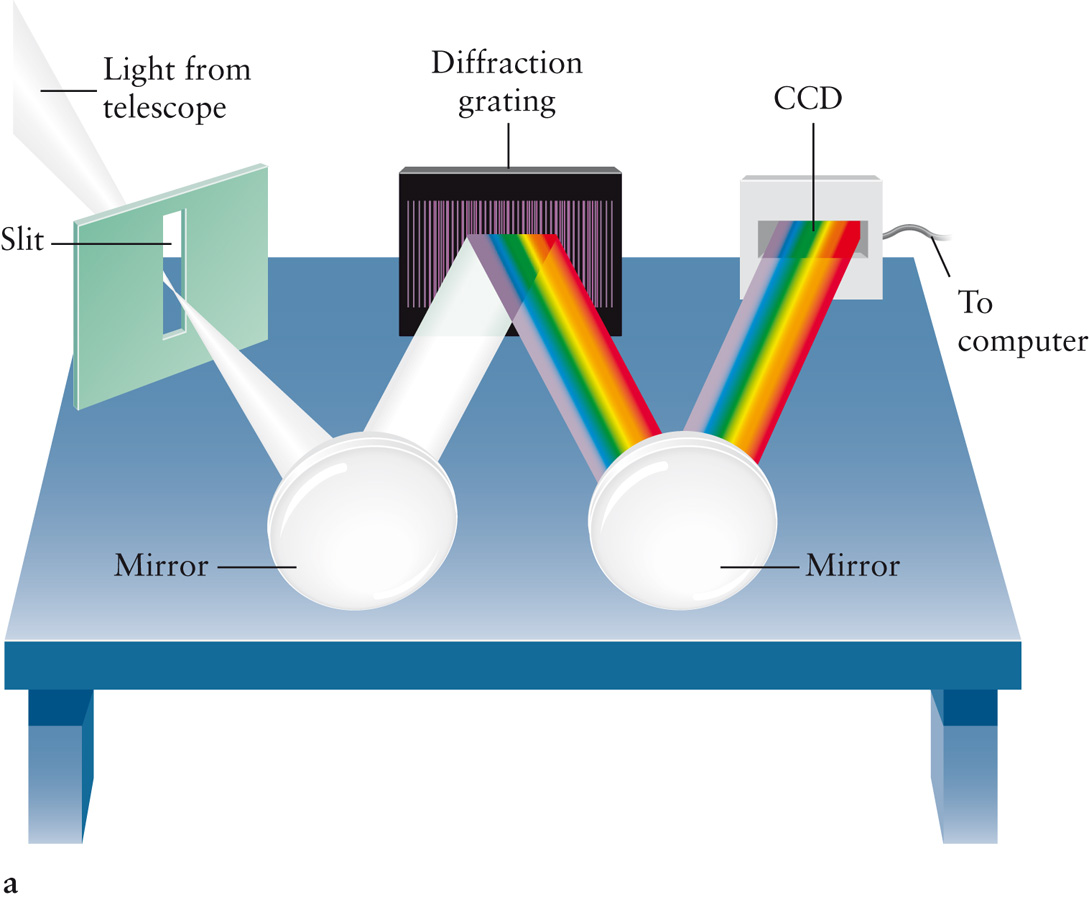
Для точного исследования спектров такие простые приспособления, как узкая щель, ограничивающая световой пучок, и призма, уже недостаточны. Необходимы приборы, дающие четкий спектр, т.е. приборы, хорошо разделяющие волны различной длины и не допускающие перекрытия отдельных участков спектра. Такие приборы называют спектральными аппаратами. Чаще всего основной частью спектрального аппарата является призма или дифракционная решетка.
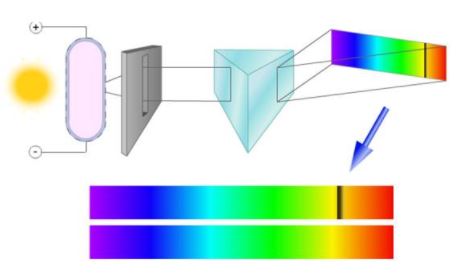
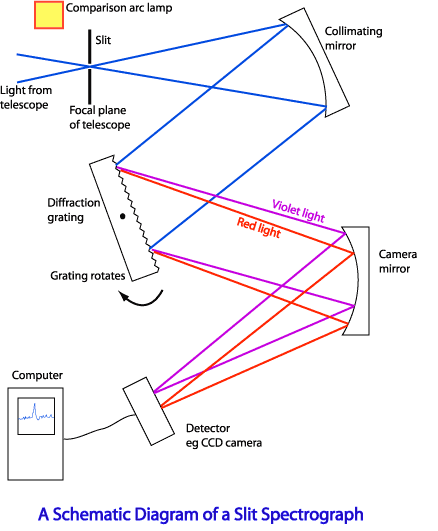
Рассмотрим схему устройства призменного спектрального аппарата. Исследуемое излучение поступает вначале в часть прибора, называемую коллиматором. Коллиматор представляет собой трубу, на одном конце которой имеется ширма с узкой щелью, а на другом — собирающая линза. Щель находится на фокусном расстоянии от линзы. Поэтому расходящийся световой пучок, попадающий на линзу из щели, выходит из нее параллельным пучком и падает на призму.
Так как разным частотам соответствуют различные показатели преломления, то из призмы выходят параллельные пучки, не совпадающие по направлению. Они падают на линзу. На фокусном расстоянии этой линзы располагается экран — матовое стекло или фотопластинка. Линза фокусирует параллельные пучки лучей на экране, и вместо одного изображения щели получается целый ряд изображений. Каждой частоте (узкому спектральному интервалу) соответствует свое изображение. Все эти изображения вместе и образуют спектр.
Описанный прибор называется спектрографом . Если вместо второй линзы и экрана используется зрительная труба для визуального наблюдения спектров, то прибор называется спектроскопом .
Применение спектрального анализа
Линейчатые спектры играют особо важную роль, потому что их структура прямо связана со строением атома. Ведь эти спектры создаются атомами, не испытывающими внешних воздействий. Состав сложных, главным образом органических смесей анализируется по их молекулярным спектрам.
С помощью спектрального анализа можно обнаружить данный элемент в составе сложного вещества , если даже его масса не превышает 10 -10 г. Линии, присущие данному элементу, позволяют качественно судить о его наличии. Яркость линий дает возможность (при соблюдении стандартных условий возбуждения) количественно судить о наличии того или иного элемента.
Спектральный анализ можно проводить и по спектрам поглощения. В астрофизике по спектрам можно определить многие физические характеристики объектов : температуру, давление, скорость движения, магнитную индукцию и др. с помощью спектрального анализа определяют химический состав руд и минералов.
Основные направления применения спектрального анализа таковы: физико-химические исследования; машиностроение, металлургия; атомная индустрия; астрономия, астрофизика; криминалистика.
Современные технологии создания новейших строительных материалов (металлопластиковые, пластиковые) непосредственно взаимосвязаны с такими фундаментальными науками как химия, физика. Данные науки используют современные методы исследования веществ. Поэтому спектральный анализ можно применять для определения химического состав состава строительных материалов по их спектрам.
Источник
Спектр солнца это сплошной спектр
На 1 квадратный метр обращенной к Солнцу поверхности площадки в окрестностях Земли ежесекундно поступает 1400 Дж энергии, переносимой солнечным электромагнитным излучением. Эта величина называется солнечной постоянной . Иными словами, плотность потока энергии солнечного излучения составляет 1,4 кВт/м 2 .
Впервые для определения солнечной энергии был использован метод измерения нагревающего действия солнечных лучей Пулье (1837 год). Такой прибор называется пиргелиометром . В пиргелиометре находилась вода, температуру которой измерял обычный термометр. Под действием солнечных лучей температура воды возрастала.
Спектр Солнца непрерывный, в нем наблюдается множество темных фраунгоферовых линий . Фраунгофер был первым, кто описал темные линии на фоне непрерывного спектра в 1814 году. Эти линии в спектре Солнца образуются в результате поглощения квантов света в более холодных слоях солнечной атмосферы.
 1 1 |
| Рисунок 5.1.2.1. Наибольшую интенсивность непрерывный спектр имеет в области длин волн 430–500 нм. В видимой и инфракрасной областях спектр электромагнитного излучения Солнца близок к спектру излучения абсолютно черного тела с температурой 6000 К. Эта температура соответствует температуре видимой поверхности Солнца – фотосферы. В видимой области спектра Солнца наиболее интенсивны линии Н и К ионизованного кальция, линии бальмеровской серии водорода Нα, Нβ и Нγ. Около 9 % энергии в солнечном спектре приходится на ультрафиолетовое излучение с длинами волн от 100 до 400 нм. Остальная энергия разделена приблизительно поровну между видимой (400–760 нм) и инфракрасной (760–5000 нм) областями спектра. Солнце – мощный источник радиоизлучения. В межпланетное пространство проникают радиоволны, которые излучает хромосфера (сантиметровые волны) и корона (дециметровые и метровые волны). Радиоизлучение Солнца имеет две составляющие – постоянную и переменную. Постоянная составляющая характеризует радиоизлучение спокойного Солнца. Солнечная корона излучает радиоволны как абсолютно черное тело с температурой = 10 6 К. Переменная составляющая радиоизлучения Солнца проявляется в виде всплесков, шумовых бурь. Шумовые бури длятся от нескольких часов до нескольких дней. Через 10 минут после сильной солнечной вспышки радиоизлучение Солнца возрастает в тысячи и даже миллионы раз по сравнению с радиоизлучением спокойного Солнца; это состояние длится от нескольких минут до нескольких часов. Это радиоизлучение имеет нетепловую природу. Плотность потока излучения Солнца в рентгеновской области (0,1–10 нм) весьма мала ( 5∙10 –4 Вт/м 2 и сильно меняется с изменением уровня солнечной активности. В ультрафиолетовой области на длинах волн от 200 до 400 нм спектр Солнца также описывается законами излучения абсолютно черного тела. В ультрафиолетовой области спектра с длинами волн короче 200 нм интенсивность непрерывного спектра резко падает и появляются эмиссионные линии. Наиболее интенсивна из них водородная линия лаймановской серии ( = 121,5 нм). При ширине этой линии около 0,1 нм ей соответствует плотность потока излучения около 5∙10 –3 Вт/м 2 . Интенсивность излучения в линии приблизительно в 100 раз меньше. Заметны также яркие эмиссионные линии различных атомов, важнейшие линии принадлежат Si I ( = 181 нм), Mg II и Mg I, O II, O III, C III и другие. Коротковолновое ультрафиолетовое излучение Солнца возникает вблизи фотосферы. Рентгеновское излучение исходит из хромосферы ( 10 4 К), расположенной над фотосферой, и короны ( 10 6 К) – внешней оболочки Солнца. Радиоизлучение на метровых волнах возникает в короне, на сантиметровых – в хромосфере. Источник ➤ Adblockdetector |