Этимология химических элементов
презентация к уроку по химии (8 класс) на тему
Скачать:
| Вложение | Размер |
|---|---|
| etimologiya_himicheskih_elementov.pptx | 2.54 МБ |
Предварительный просмотр:
Подписи к слайдам:
Этимология химических элементов 8 класс Учитель химии МБУ СОШ № 13 Алексеева Г. И.
Этимология — это раздел языкознания, исследующий происхождение слов разных языков [гр. «ety-mologia» etymon- истина + logos- понятие, учение]
В 1814 году появились символы и названия химических элементов, которыми химики пользуются по сей день. Шведский химик Йенс-Якоб Берцелиус предложил обозначать химические элементы первой буквой (или первой и одной из следующих букв) латинского названия элемента. Например, водород (по-латыни «гидрогениум», Hydrogenium )- Н (читается » аш «) углерод (по-латыни «карбонеум (Carboneum) — C (читается » цэ «) золото (по-латыни «аурум» Aurum) — Au (читается тоже «аурум»)
Некоторые названия отражают представления о функциях элементов в химических реакциях: водород Н «рождает» воду кислород О — кислоты. Эти названия — дословный перевод на русский с латыни ( hydrogenium , oxygenium ). Их придумал А.Л. Лавуазье, который ошибочно полагал, что кислород „рождает“ все кислоты. Логичнее было бы поступить наоборот: назвать кислород водородом (этот элемент тоже „рождает“ воду), а водород — кислородом, так как он входит в состав всех кислот .
Есть названия элементов, обязанные собой цвету простых веществ и соединений: Rb — рубидий от латинского «rubidus» (темно-красный), открыт по линиям в красной части спектра. Cl — хлор от греческого «chloros» (желто-зеленый) Именно такой цвет имеет этот газ Cs — цезий от латинского «caesius» (голубой), открыт по ярко-синим спектральным линиям I- йод назван по цвету паров: греч. iodes фиолетовый Такой цвет имеют пары этого элемента In — индий назван по синей (цвета индиго) линии спектра P- фосфор от греческого «phosphoros» (светоносный)
Очень многие элементы имеют названия, происходящие от содержащих их минералов
Некоторые элементы имеют географическое происхождение Na — натрий (от » Натрум » — имени соленого озера в Африке, где в древности добывали природную соду, карбонат натрия), Cu — медь (латинское » купрум «- Cuprum образовано от имени острова Кипр с его богатыми медными приисками).
Некоторые элементы имеют географическое происхождение Sc скандий назван от латинского «Scandia» (Скандинавский полуостров) Mg магний от названия древнего города Магнезия в Малой Азии, в окрестностях которого имеются залежи минерала магнезита
Некоторые элементы названы в честь стран и частей света, где жили их первооткрыватели, городов и даже деревень, где они были найдены. Am америций лат. Americium от слова «Америка» Bk берклий (г. Беркли, США) Eu европий от слова «Европа» Ga галлий назван от Gallia, латинского названия Франции Ge германий назван от латинского Germania (Германия), в честь родины К. А. Винклер
Po полоний от латинского «Polonia» (Польша) Ru рутений от позднелатинского «Ruthenia» (Россия) Fr франций назван по имени Франции, родины М. Пере, открывшей элемент Te теллур название от латинского » tellus «, родительный падеж «telluris» (Земля) Se селен от греческого » selene » (Луна) He гелий — от греческого » гелиос » — солнце).
В Периодической системе элементов можно найти имена богов и героев Древней Греции тантал Ta титан Ti прометий Pm скандинавская богиня весны Ванадис — ванадий V ниобий Nb назван от имени Ниобы, дочери мифологического Тантала
Названия планет Солнечной системы U уран от планеты Уран Pu плутоний от планеты Плутон Np нептуний от планеты Нептун Pd палладий назван по планете Паллада
Названия, характеризующие свойства Ar — аргон от греческого «argos» (недеятельный) As — мышьяк лат. Arsenicum , русское название от слова «мышь» (препараты мышьяка применялись для истребления мышей и крыс). Ba — барий от греческого » barys » (тяжелый) Br — бром от греческого «bromos» — зловоние. Удушающий запах брома похож на запах хлора. Dy — диспрозий от греческого «dysprositos» (труднодоступный) Ne -неон от греческого « neos » — новый F – фтор от греч. „фторос“ — разрушение, гибель.
Ir- иридий от греческого «iris» (радуга) Kr -криптон от греческого «kryptos» (скрытый), в связи с трудностями получения La — лантан назван от греческого «lanthano» (скрываюсь), в связи с трудностями получения N -азот название от греческой a (отрицательная приставка) и zoe — жизнь (безжизненный) Pt -платина от испанского «platina» (уменьшительное от «plata» — серебро) Ra — радий от латинского «radius» (луч) Os -осмий назван от греческого «osme» (запах), по резко пахнущему, похожим на запах хлора и чеснока, оксиду OsO 4
Химические элементы, названные в честь исследователей Bh — борий назван в честь Нильса Бора, датского физика
Химические элементы, названные в честь исследователей Cm -кюрий назван в честь Пьера Кюри и Мари Склодовской-Кюри В символе элемента ( Cm ) первая буква обозначает фамилию Кюри, вторая — имя Марии.
Химические элементы, названные в честь исследователей Es — эйнштейний назван по имени физика Альберта Эйнштейна
Химические элементы, названные в честь исследователей Fm — фермий назван по имени физика Энрико Ферми
Химические элементы, названные в честь исследователей Gd — гадолиний назван по имени финского химика Юхана Гадолина. Это был первый случай, когда химический элемент назвали в честь учёного, открывшего его.
Химические элементы, названные в честь исследователей Lr — лоуренсий назван по имени Эрнеста Орландо Лоуренса, американского физика
Химические элементы, названные в честь исследователей Mt — мейтнерий назван в честь Лизы Мейтнер австрийского физика
Химические элементы, названные в честь исследователей No — нобелий название дано шведскими учеными по имени Альфреда Нобеля
Химические элементы, названные в честь исследователей Rf — резерфордий назван в честь химика и физика Эрнеста Резерфорда
Химические элементы, названные в честь исследователей Sg — сиборгий назван в честь Гленна Теодора Сиборга , американского специалиста по ядерной химии и лауреата Нобелевской премии
Химические элементы, названные в честь исследователей М d — Менделевий Назван в честь Д.И. Менделеева.
По теме: методические разработки, презентации и конспекты
Разработка урока химии в 8 классе «Знаки химических элементов. Периодическая система Д.И.Менделеева» с применением образовательных технологий.
Материал для учителей, работающих по программе О.С.Габриеляна.
Комбинированный урок с применением ЭОР.
Проверочная работа по теме «Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Относительная атомная и молекулярная массы» предназначена дл.
Проверочная работа по теме «Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Аr и Mr» предназначена для учащихся 8 классов. Она включает.
На таких уроках реализую межпредметные связи. А так же осуществляю интегрированный подход. Очень люблю историю химии. Вместе с детьми готовим презентации, в которых отображаем накопленный челове.
Источник
Презентация по химии на тему «Химические элементы в космосе» (10 класс)
Описание презентации по отдельным слайдам:
Выполнили работу: Шаркова Виктория Мелехова Валерия ученицы 10 «А» класса Руководитель: Павлова Е.П. учитель химии и биологии ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ В КОСМОСЕ
Людей всегда манили дали, Их вечно звали океаны. А космос жил не торопясь, Он был загадочен и страшен. И только звезды русских башен Держали с ним прямую связь.
ЦЕЛЬ: Изучить химию планет и звезд ЗАДАЧИ: Познакомиться с материалом по данной теме и с наукой Космохимией. Узнать и рассказать о новых и интересных фактах космической химии. Использовать полученные знания в дальнейшем.
Алхимия Занятия астрологией были тесно связаны с алхимическими опытами, которые находили взаимосвязь со всеми процессами Космоса.
Алхимия Космические «двойники»: Золоту соответствовало Солнце Серебру – Луна Ртути – Меркурий Меди – Венера Железу – Марс Олову – Юпитер Свинцу – Сатурн
Химические элементы и небесные тела Селен (Se) № 34 – назван в честь Луны Теллур (Te) № 52 – в честь Земли Уран (U) № 92 – в честь Урана Нептуний (Np) № 93 – в честь Нептуна Плутоний (Pu) № 94 – в честь Плутона Церий (Ce) № 58 – в честь Цереры
КОСМОХИМИЯ Наука изучающая химический состав космических тел и веществ, заполняющего космическое пространство, законы распространения химических элементов во Вселенной, процессы образования и миграции космического вещества.
Состав земной коры O – 46.6 % Ca – 3.63 % Al – 8.13 % Na – 2.83 % Si – 27.72 % K – 2.59 % Fe – 5.0 % Mg – 2.0 % Всего — 98,59%
Периодическая система химических элементов Д. И. Менделеева
Метеорит Гоба — крупнейший метеорит. Самый большой на Земле кусок железа природного происхождения.
Химический состав метеорита Состоит из наиболее распространенных на Земле химических элементов: железа, кислорода, кремния, магния, алюминия, кальция — (94%) . Состав метеоритов равен составу земного шара.
Состав планет Меркурий – 70% металлов и 30% силикатной породы Венера – силикатные породы (в ядре никель + железо) Марс – состоит из железа и его сплавов + силикатная порода
Классный час в 10 А
Выводы космохимия – наука о химическом составе космических тел; все небесные тела построены из небольшого числа обычных химических элементов; проведены классные часы по данной теме в нашей школе.
Литература Демин В.Н. Тайны Вселенной. – М., 1997. Происхождения названий химических элементов и терминов. И.А. Леенсон, «Химия и жизнь – 21 век». Рубцова А.Д. «Этимология названий химических элементов. – М., 2001 Уразов И.А. Почему мы так говорим. – М., 1996. Трифонов Д.Н., Трифонов В.Д. Как были открыты химические элементы. – М.,1980 Фигуровский Н.А.«Открытие элементов и происхождение их названий». – Москва, Наука, 1970.
Номер материала: ДБ-775843
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Минобрнауки рекомендовало своим организациям вакцинировать сотрудников
Время чтения: 1 минута
Второе высшее образование в творческих вузах станет бесплатным
Время чтения: 1 минута
Петербургская школьница набрала 300 баллов на ЕГЭ
Время чтения: 1 минута
Путин поручил разработать программу содействия занятости молодежи
Время чтения: 1 минута
Глобальная программа строительства школ охватит большинство регионов России
Время чтения: 1 минута
Минобрнауки прорабатывает идею создания центра истории Великой Отечественной войны
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Источник
Презентация на тему Происхождение химических элементов
Презентация на тему Происхождение химических элементов из раздела Разное. Доклад-презентацию можно скачать по ссылке внизу страницы. Эта презентация для класса содержит 58 слайдов. Для просмотра воспользуйтесь удобным проигрывателем, если материал оказался полезным для Вас — поделитесь им с друзьями с помощью социальных кнопок и добавьте наш сайт презентаций TheSlide.ru в закладки!
Слайды и текст этой презентации
Лекция 2
Происхождение химических элементов.
Атомы состоят из нуклонов (протонов и нейтронов) в ядре, окруженных электронами.
Число протонов определяет атомный номер Z (характеристика элемента).
Число протонов Z и нейтронов N определяет атомную массу элемента А.
Протоны заряжены положительно, нейтроны не имеют заряда, электроны – отрицательно.
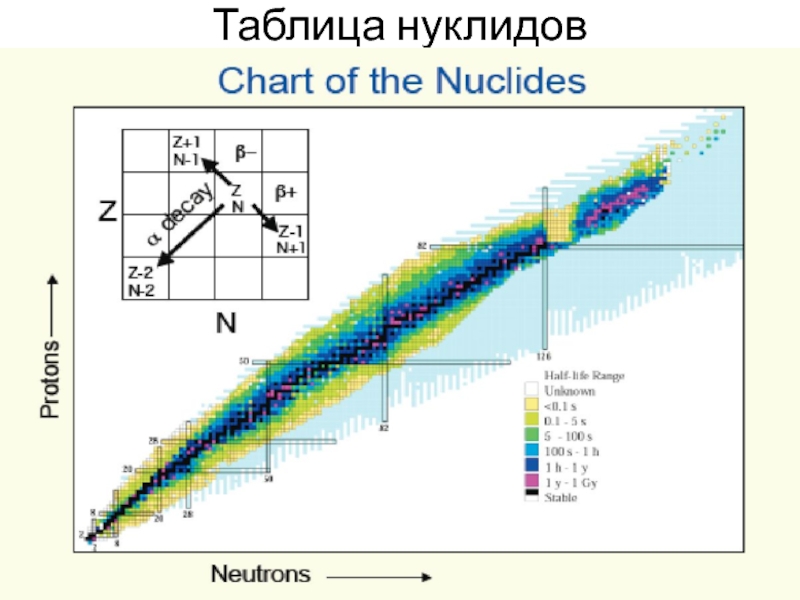
Нуклиды — атомы, различающиеся числом нуклонов в ядре или, при одинаковом числе нуклонов, содержащие разное число протонов или нейтронов.
Атомы с четным количеством протонов и нейтронов более стабильны по сравнению с атомами, где количество тех или иных нуклонов нечетное.
Особенно стабильны атомы с «магическими числами» протонов или нейтронов (четное число и протонов, и нейтронов).
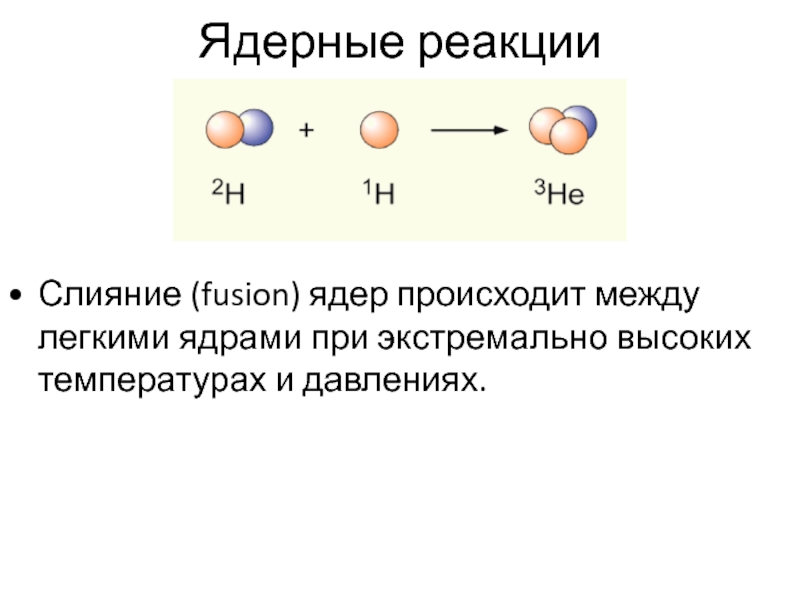
Слияние (fusion) ядер происходит между легкими ядрами при экстремально высоких температурах и давлениях.
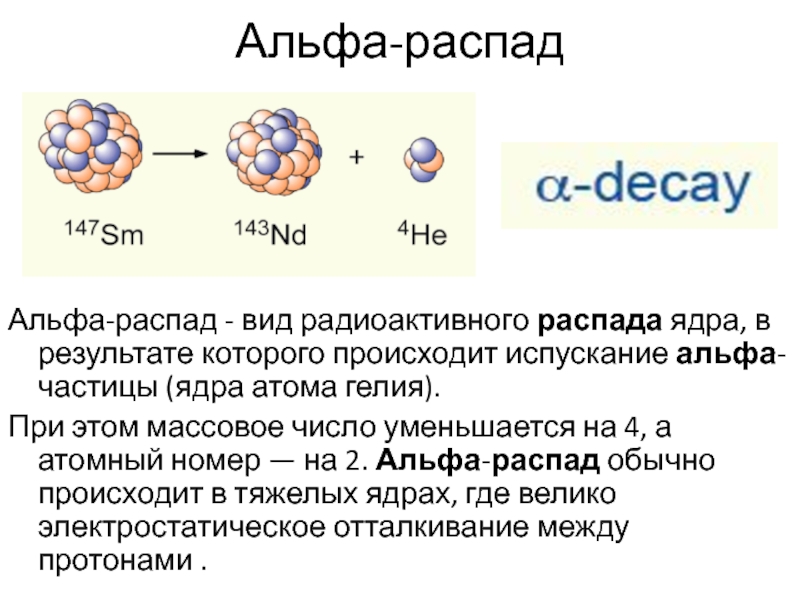
Альфа-распад — вид радиоактивного распада ядра, в результате которого происходит испускание альфа-частицы (ядра атома гелия).
При этом массовое число уменьшается на 4, а атомный номер — на 2. Альфа-распад обычно происходит в тяжелых ядрах, где велико электростатическое отталкивание между протонами .
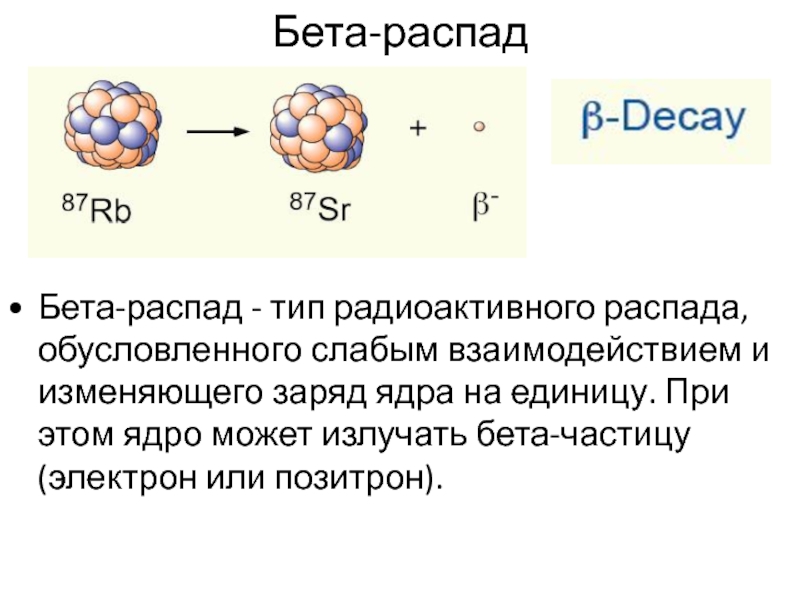
Бета-распад — тип радиоактивного распада, обусловленного слабым взаимодействием и изменяющего заряд ядра на единицу. При этом ядро может излучать бета-частицу (электрон или позитрон).
В случае испускания электрона он называется «бета-минус» (β−), а в случае испускания позитрона — «бета-плюс-распадом» (β+).
Кроме β− и β+ распадов, к бета-распадам относят также электронный захват, когда ядро захватывает атомный электрон.
Во всех типах бета-распада ядро излучает электронное нейтрино (β+ распад, электронный захват) или антинейтрино (β− распад).
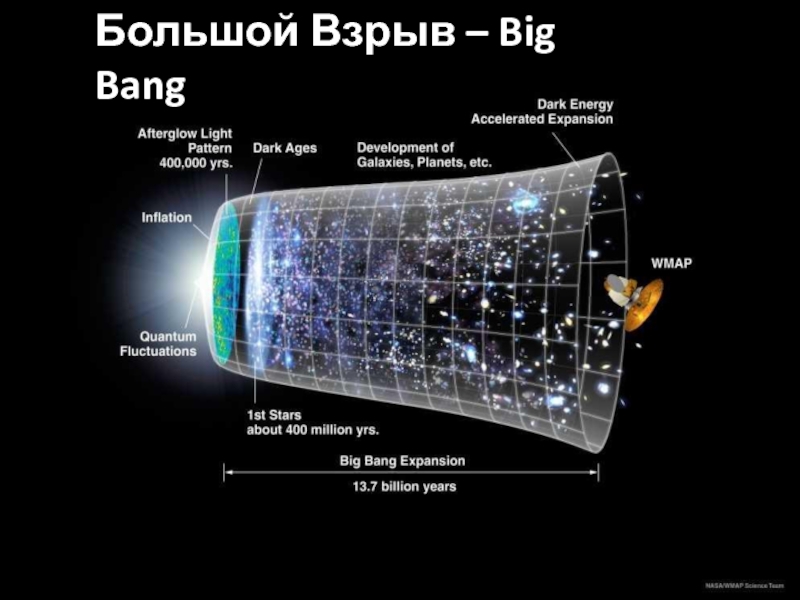
Большой Взрыв – Big Bang
Вселенная в целом расширяется с ускорением и в буквальном смысле слова «в никуда». Иными словами, галактики не просто разлетаются в разные стороны в пустом пространстве, а раздвигается само пространство: наиболее часто этот процесс ученые иллюстрируют примером воздушного шарика.
Возраст Вселенной
13.75 +/- 0.17 Ga
определен с помощью гравитационной линзы и метода, предложенного 45 лет назад норвежцем Рефсдалем.
Иллюстрация гравитационной линзы — свет от далекой галактики отклоняется некоторым массивным объектом и в результате астрономы видят не одно изображение, а несколько. Белые стрелки показывают путь света, оранжевые — кажущееся направление на галактику.
Другие методы —анализ реликтового излучения, электромагнитного излучения, возникшего при Большом Взрыве, наблюдения за вспышками далеких сверхновых.
После первой секунды после Большого Взрыва материя присутствовала в виде протонов, нейтронов и электронов.
Температура достигала 1010 К.
Через несколько минут, когда T понизилась до 109 K,протоны и нейтроны начали образовывать легкие атомы 2H, 3He, 4He и 7Li.
Вычисленные заранее количества нуклидов хорошо согласуются с наблюдаемыми в космосе содержаниями.
В процессе первичного нуклеосинтеза образуются элементы не тяжелее Li.
Солнце (98% массы Солнечной системы) состоит из 71% H, 27% He – результат Большого Взрыва, 2% более тяжелых элементов, образованных в предшествующих звездах и суперновых после Большого Взрыва). Поэтому Солнце является звездой второго поколения.
Примерно через 100 000 лет при понижении T до 5000 K начинают образовываться нейтральные атомы H и He.
Образование звезд и звездный нуклеосинтез
Звезды образуются при гравитационной конденсации водородного облака.
Высокие температуры и давления допускают ядерные реакции – слияние ядер.
Образование звезды
в туманности Орион
(NASA, телескоп Хаббла)
Проблема происхождения атомов возникла при установлении природы источника энергии Солнца и звезд и при разработке теории Большого Взрыва Вселенной.
Проблема источника энергии на Солнце была решена в конце 30-х годов XX века Х. Бете и К. Вейцзекером.
На основе расчетов они пришли к выводу, что механизм генерации энергии на Солнце и в других звездах связан с образованием ядер гелия из четырех протонов.
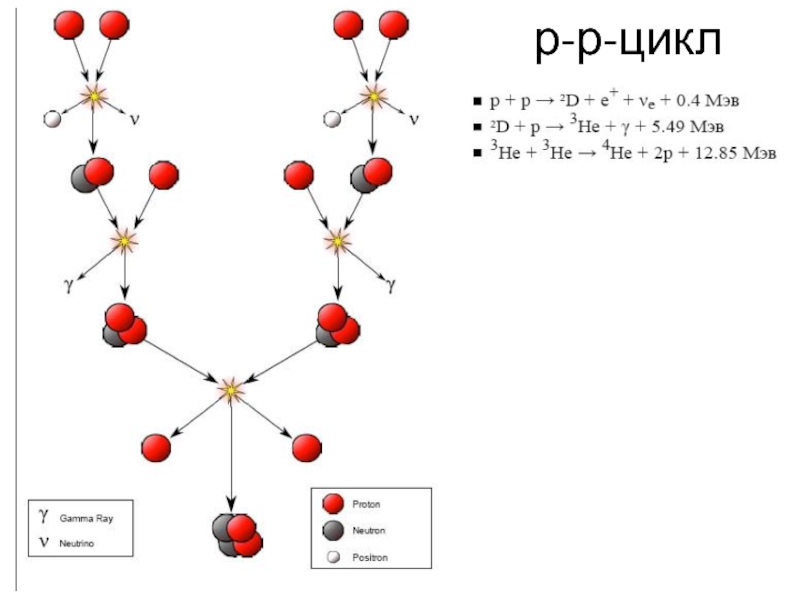
Протон-протонный цикл — совокупность цепочек термоядерных реакций, в ходе которох водород превращается в гелий в звёздах, находящихся на главной звездной последовательности, основная альтернатива CNO-циклу.
Доминирует в звёздах с массой порядка Солнца или меньше.
Время, через которое Солнце израсходует своё «топливо» и термоядерная реакция прекратится, оценивается в 6 миллиардов лет.
Суммарным итогом реакции является слияние четырех протонов с образованием ядра атома He и выделением энергии, эквивалентной 0,7 % массы этих протонов.
Эта реакция проходит в три стадии. Вначале два протона, имеющие достаточно энергии, чтобы преодолеть кулоновский барьер, сливаются, образуя дейтрон, позитрон и электронное нейтрино; затем дейтрон сливается с протоном, образуя ядро 3He; наконец, два ядра атома гелия-3 сливаются, образуя ядро атома гелия-4. При этом высвобождается два протона.
CNO-цикл — термоядерная реакция превращения водорода в гелий, в которой углерод, кислород и азот выступают как катализаторы.
Считается одним из основных процессов термоядерного синтеза в массивных звёздах главной последовательности.
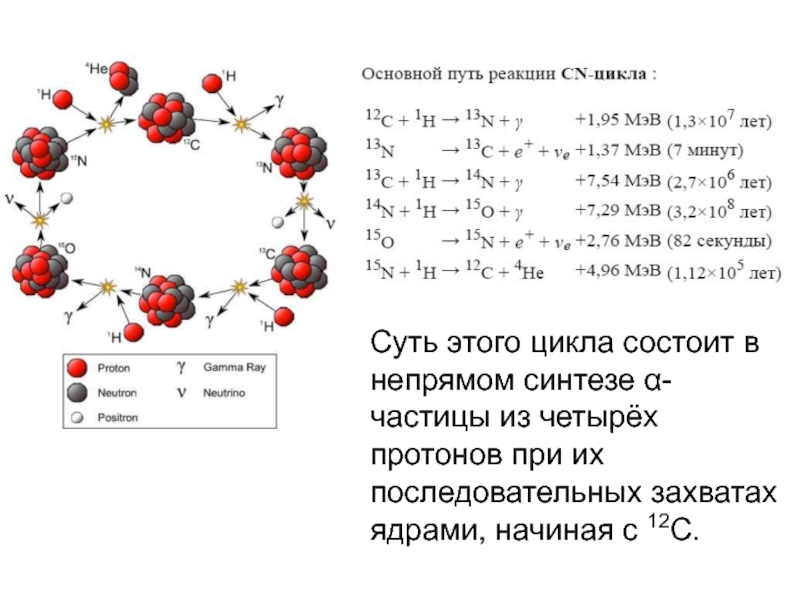
CNO-цикл — это совокупность трёх сцепленных друг с другом или, точнее, частично перекрывающихся циклов. Самый простой из них CN-цикл (цикл Бете или углеродный цикл) был предложен Хансом Бете в 1938 г. и, независимо от него, Карлом Вайцзекером.
Суть этого цикла состоит в непрямом синтезе α-частицы из четырёх протонов при их последовательных захватах ядрами, начиная с 12C.
Звёздный нуклеосинтез — собирательное понятие для ядерных реакций образования элементов тяжелее H, внутри звёзд, а также, в незначительной степени на их поверхности.
М. Бeрбидж, Г. Бeрбидж, В. Фаулер, Ф. Хойл в 1957 году указали основные процессы зёздной эволюции, в которых происходит образование атомных ядер. К процессам звёздного нуклеосинтеза относятся:
Альфа-процесс (α-процесс) — ядерная реакция захвата α-частиц ядрами лёгких элементов. В звёздах он является основным источником производства элементов от He до Ni.
Образование тяжелых и сверхтяжелых элементов
Синтез атомных ядер, расположенных в таблице Д. Менделеева за группой железа, должен обеспечиваться другими механизмами и, как показали М. и Дж. Бербиджи, У. Фаулер и Ф. Хойл еще в 1957 году, такие нуклиды образуются в результате трех принципиально разных процессов: s-,r- и p-процессов.
Эти процессы сокращенно названы по первым буквам фамилий первооткрывателей: B2FH
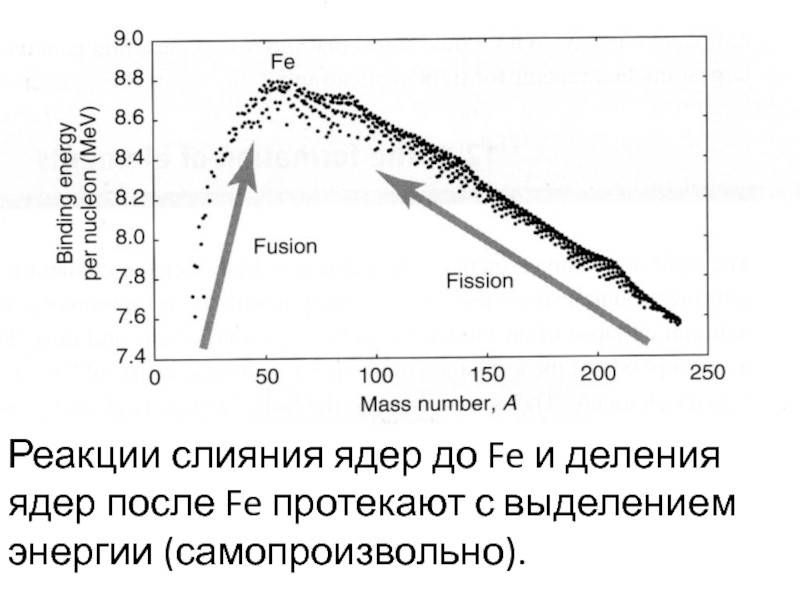
График энергии
связи нуклонов
Элементы >Fe не синтезировать прямым слиянием
Реакции слияния ядер до Fe и деления ядер после Fe протекают с выделением энергии (самопроизвольно).
Этот процесс представляет собой медленный захват нейтронов, при котором образующиеся неустойчивые ядра распадаются прежде, чем успеют присоединить следующий нейтрон.
Поэтому можно заключить, что s-процесс идет в недрах звезд при их нормальной стадии эволюции.
В звездах – Красных гигантах – горение O и Si производит значительный поток нейтронов. Они могут быть захвачены ядрами для образования новых изотопов с массой более 56.
Но ядра 59Fe не стабильны и распадаются на 59Co с превращением нейтрона в протон и испусканием гамма-кванта.
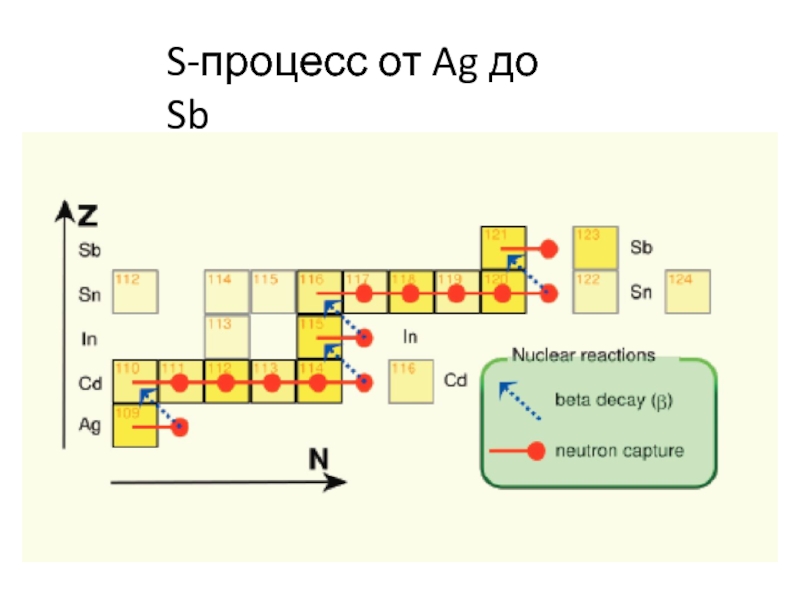
S-процесс от Ag до Sb
Завершаются цепочки превращений -процесса на изотопах свинца и висмута 209Bi, так как последующие нуклиды 210Рo и 211Рo претерпевают -распад с периодом полураспада 138 суток и 0,5 с соответственно, превращаясь в свинец.
Тяжелые и сверхтяжелые элементы, находящиеся в таблице Менделеева за Bi, образуются в результате r-процесса. В этом процессе ядро должно быстро последовательно захватить много нейтронов, прежде чем произойдет его beta—распад.
Захваты продолжаются до тех пор, пока скорость реакции захвата не уравновесится со скоростью реакции выбивания нейтрона под действием gamma-фотона (либо скоростью beta- -распада).
После этого ядро «ждет», пока произойдет beta—распад, что позволит ему снова захватить нейтроны.
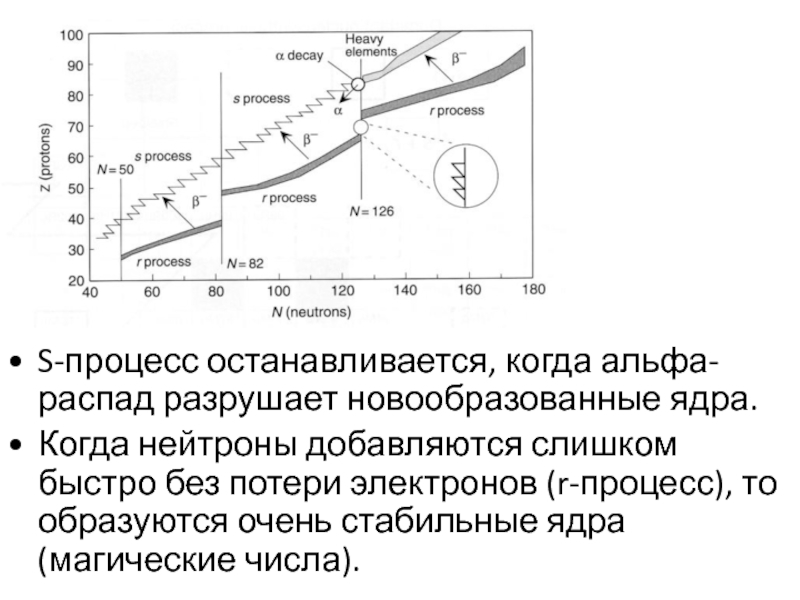
S-процесс останавливается, когда альфа-распад разрушает новообразованные ядра.
Когда нейтроны добавляются слишком быстро без потери электронов (r-процесс), то образуются очень стабильные ядра (магические числа).
Представляет собой образование редких, богатых протонами ядер путем захвата протонов или позитронов, так как ни одним процессом нейтронного захвата эти ядра не могут быть созданы.
К таким ядрам следует в первую очередь отнести изотопы олова 111Sn, 112Sn и 115Sn.
Однако физические модели условий протекания p-процесса в звездах остаются пока в большей степени неоднозначными по сравнению с процессами захвата нейтронов
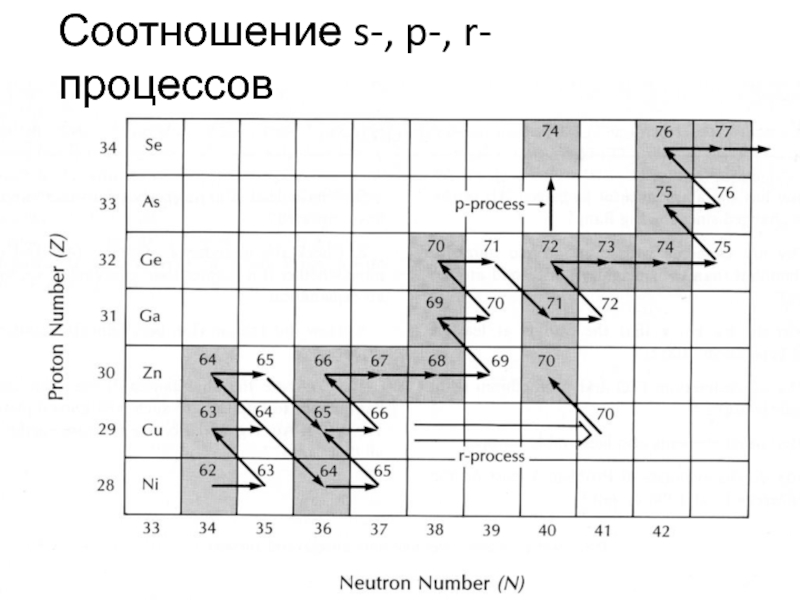
Соотношение s-, p-, r- процессов
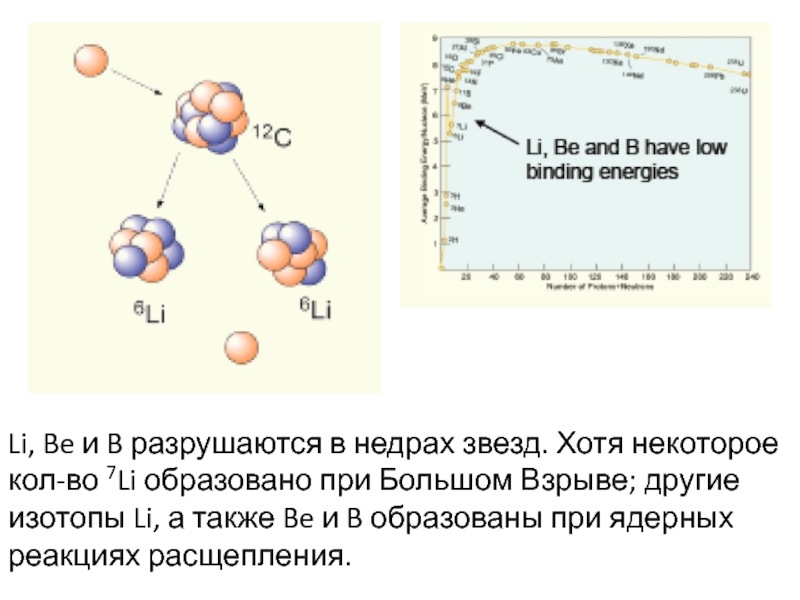
Происхождение легких элементов
Легкие нуклиды 6Li, 7Li, 9Be, 10B и 11B характеризуются более низкой распространенностью и стабильностью по отношению к He, C, N, O и не могут образоваться в процессе обычного нуклеосинтеза в недрах звезд, так как они легко разрушаются.
На сегодняшний день общепризнанной гипотезой образования легких ядер являются реакции скалывания — реакции деления ядер C, N, O при столкновении с ядрами H и He либо в космических лучах, либо космических лучей с атомами межзвездных газовых облаков.
Космические лучи — это поток заряженных частиц, включая ядра ряда атомов (H, He) достаточно большой энергии, которые заполняют пространство Галактики. Считается, что основным источником космических лучей являются взрывы сверхновых звезд. В космических лучах содержание Li, Be, B приблизительно на пять порядков больше, чем в звездах. Это указывает на то, что реакции скалывания имеют место в космических лучах.
Li, Be и B разрушаются в недрах звезд. Хотя некоторое кол-во 7Li образовано при Большом Взрыве; другие изотопы Li, а также Be и B образованы при ядерных реакциях расщепления.
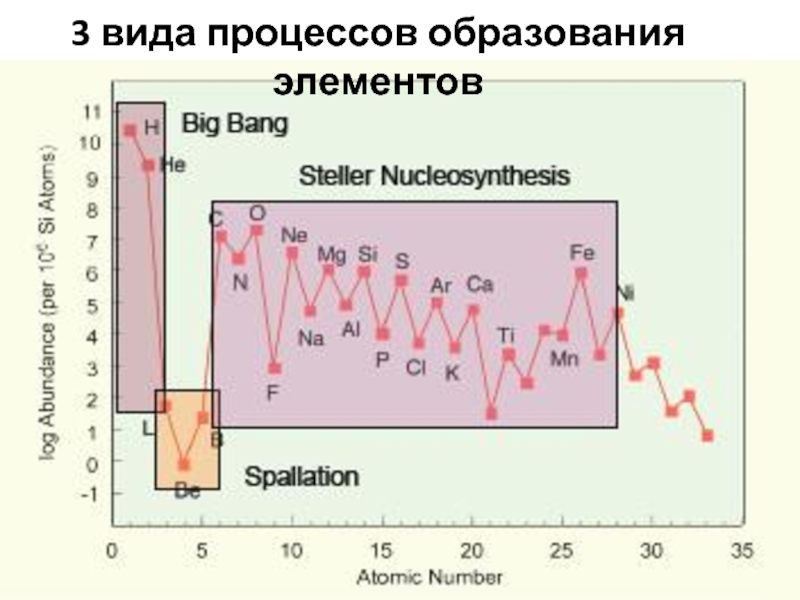
3 вида процессов образования элементов
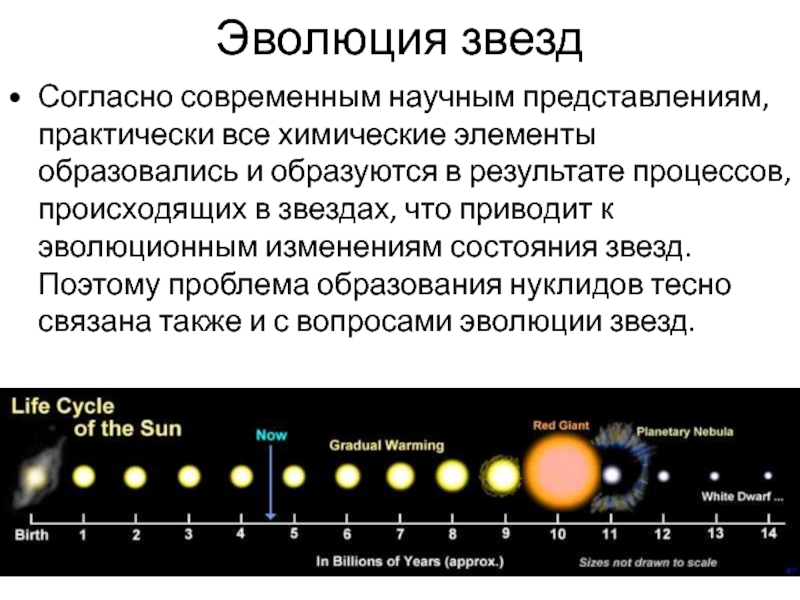
Согласно современным научным представлениям, практически все химические элементы образовались и образуются в результате процессов, происходящих в звездах, что приводит к эволюционным изменениям состояния звезд.Поэтому проблема образования нуклидов тесно связана также и с вопросами эволюции звезд.
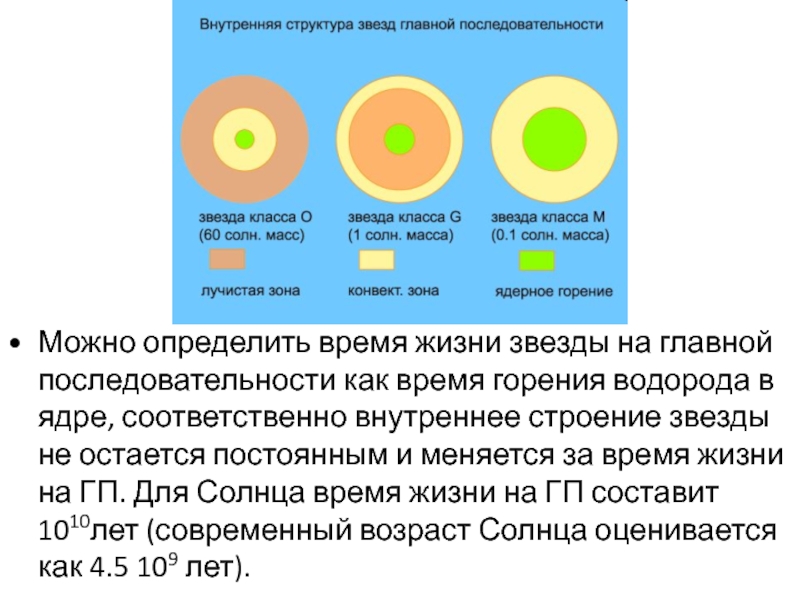
Можно определить время жизни звезды на главной последовательности как время горения водорода в ядре, соответственно внутреннее строение звезды не остается постоянным и меняется за время жизни на ГП. Для Солнца время жизни на ГП составит 1010лет (современный возраст Солнца оценивается как 4.5 109 лет).
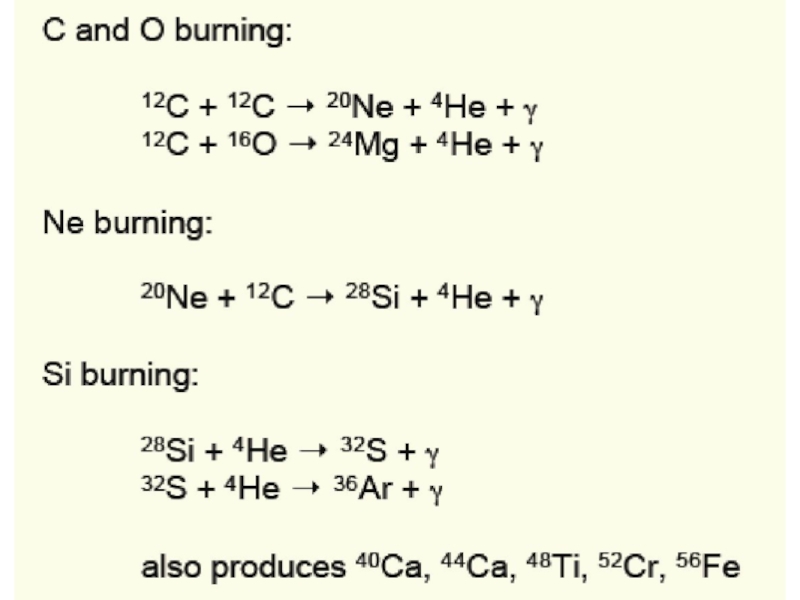
Когда весь водород использован, то звезда вступает в фазу развития Красного гиганта (T = 108K ρ = 104 g cm-3 ) со следующими реакциями:
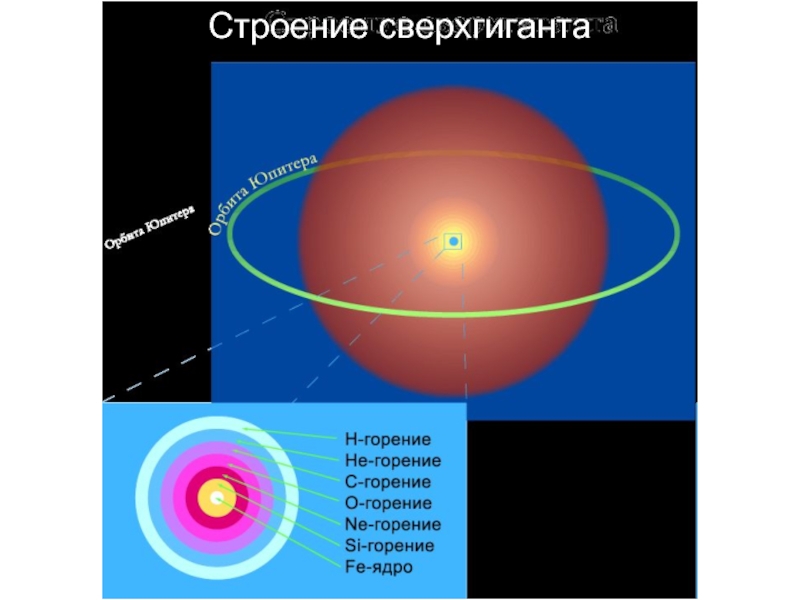
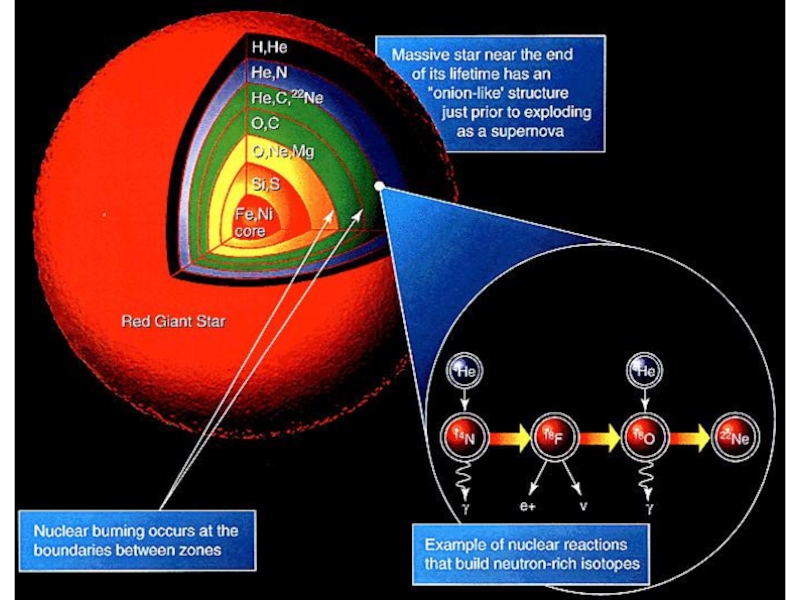
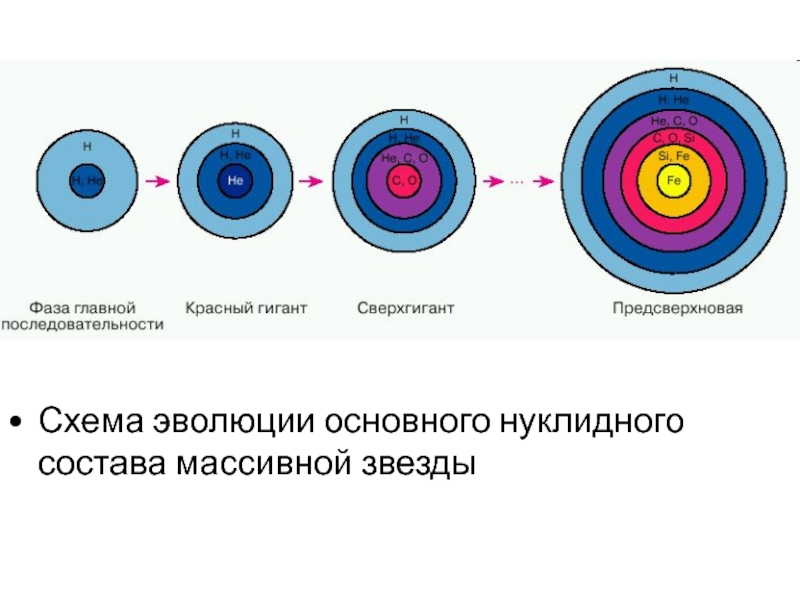
Сверхгиганты, находящиеся на последних стадиях эволюции (красные сверхгиганты), имеют весьма сложное строение, в чем-то напоминающее строение луковицы в разрезе.
Как известно из теории эволюции звезд на основе ядерных превращений в ядре звезды будут синтезироваться все новые и новые элементы, вплоть до элементов железного пика. В тоже время будет продолжаться горение элементов в слоевых источниках вокруг ядра. В сложном, далеко проэволюционировавшем сверхгиганте будет инертное Fe ядро и последовательные горящие оболочки из Si, Ne, O, C, He и H.
Железный пик — элементы группы железа от скандия Sc до никеля Ni, до которых совершаются ядерные превращения в ядрах массивных звезд. В ядрах звезд эти реакции идут с выделением энергии. Для синтеза более тяжелых элементов в звезде необходима затрата энергии и при обычных условиях в ядрах звезд такой синтез не происходит.
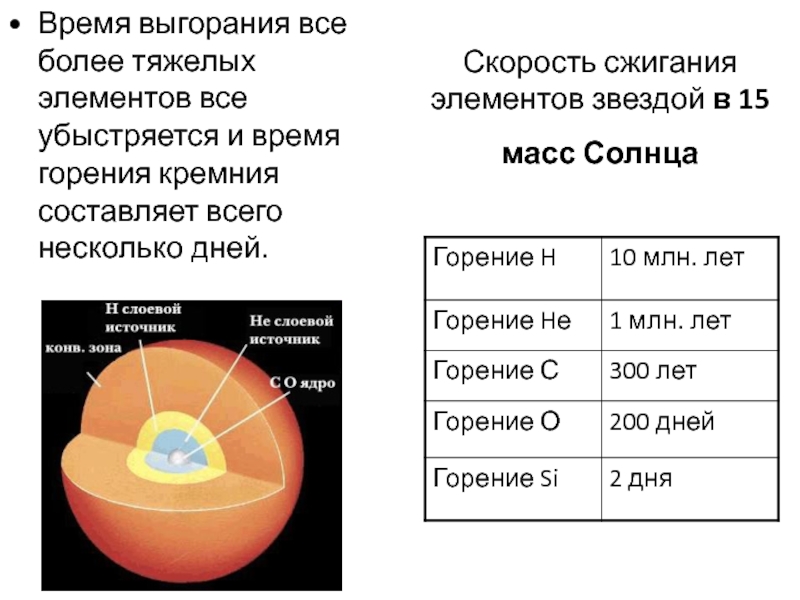
Скорость сжигания элементов звездой в 15 масс Солнца
Время выгорания все более тяжелых элементов все убыстряется и время горения кремния составляет всего несколько дней.
Схема эволюции основного нуклидного состава массивной звезды
Нуклеосинтез в разных типах звезд
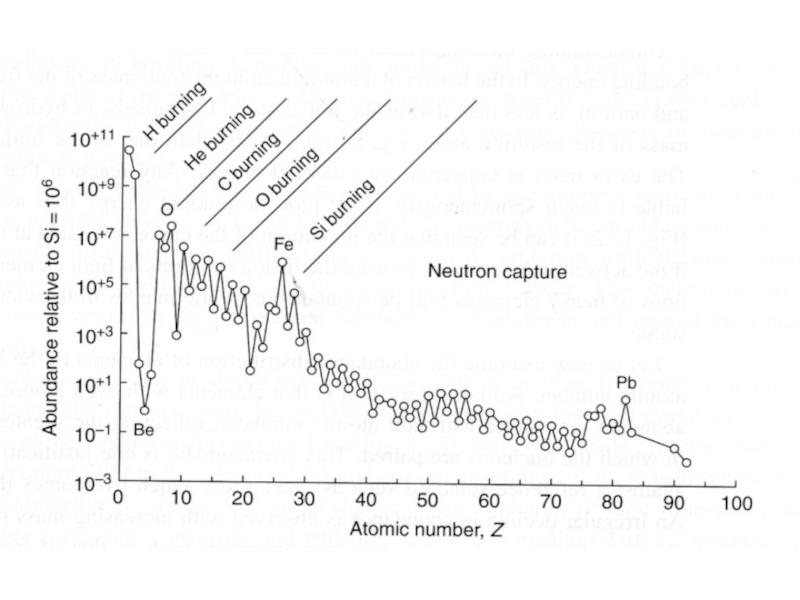
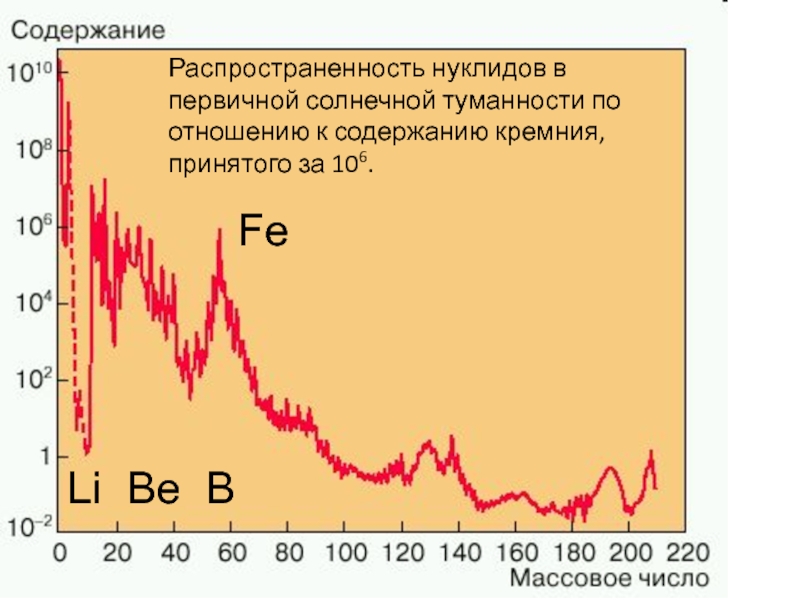
Распространенность нуклидов в первичной солнечной туманности по отношению к содержанию кремния, принятого за 106.
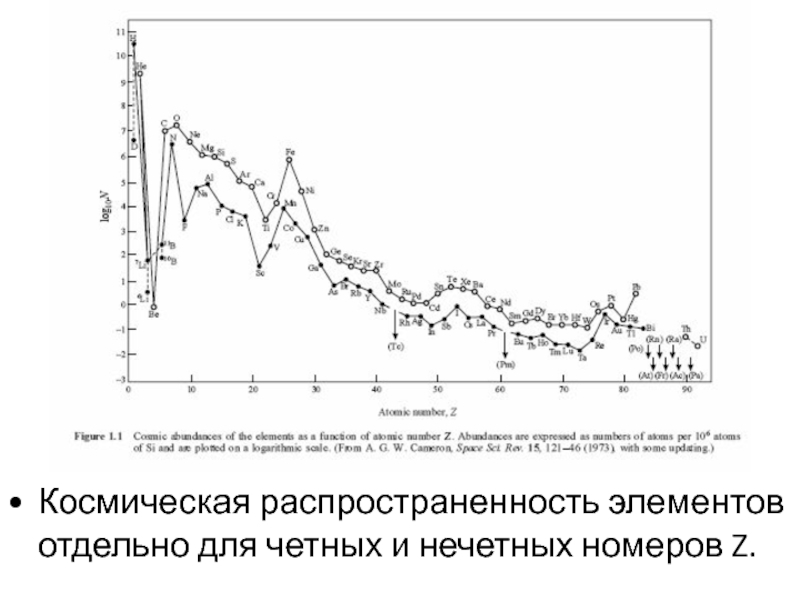
Космическая распространенность элементов отдельно для четных и нечетных номеров Z.
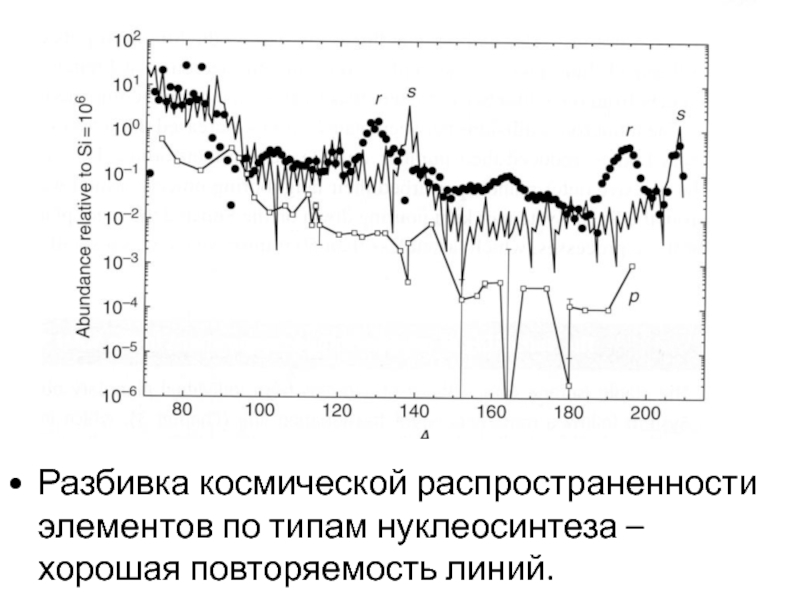
Разбивка космической распространенности элементов по типам нуклеосинтеза – хорошая повторяемость линий.
Источник